Mục Lục Bài Viết
Phạm vi áp dụng
- Nghị định này quy định về việc quản lý TTBYT bao gồm: phân loại TTBYT; sản xuất, nghiên cứu lâm sàng, lưu hành, mua bán, xuất khẩu, nhập khẩu, cung cấp dịch vụ TTBYT; thông tin, quảng cáo TTBYT; quản lý giá TTBYT và quản lý, sử dụng TTBYT tại các cơ sở y tế.
- Nghị định này không áp dụng đối với:
- Nguyên vật liệu, bán thành phẩm để sản xuất TTBYT, trừ nguyên liệu có chứa chất ma túy và tiền chất;
- Nguyên liệu sản xuất TTBYT là mẫu máu, huyết thanh, huyết tương, nước tiểu, phân, dịch tiết cơ thể người, các mẫu khác từ người khi nhập khẩu, xuất khẩu phải bảo đảm an toàn sinh học theo quy định của pháp luật;
- Khí y tế;
- Phụ kiện sử dụng cùng TTBYT;
- Các sản phẩm dùng trong y tế với mục đích nghiên cứu (Research Use Only – RUO), các sản phẩm dùng trong phòng thí nghiệm (Laboratory Use)
Định nghĩa, khái niệm về trang thiết bị y tế
1.Trang thiết bị y tế là các loại thiết bị, vật tư cấy ghép, dụng cụ, vật liệu, thuốc thử và chất hiệu chuẩn in vitro, phần mềm (software) đáp ứng đồng thời các yêu cầu sau đây:
a) Được sử dụng riêng lẻ hay phối hợp với nhau theo chỉ định của chủ sở hữu trang thiết bị y tế để phục vụ cho con người nhằm một hoặc nhiều mục đích sau đây:
- Chẩn đoán, ngăn ngừa, theo dõi, điều trị và làm giảm nhẹ bệnh tật hoặc bù đắp tổn thương, chấn thương;
- Kiểm tra, thay thế, điều chỉnh hoặc hỗ trợ giải phẫu và quá trình sinh lý
- Hỗ trợ hoặc duy trì sự sống
- Kiểm soát sự thụ thai;
- Khử khuẩn trang thiết bị y tế;
- Cung cấp thông tin cho việc chẩn đoán, theo dõi, điều trị thông qua biện pháp kiểm tra các mẫu vật có nguồn gốc từ cơ thể con người.
b) Không sử dụng cơ chế dược lý, miễn dịch hoặc chuyển hóa trong hoặc trên cơ thể người hoặc nếu có sử dụng các cơ chế này thì chỉ mang tính chất hỗ trợ để đạt mục đích quy định tại điểm a khoản này.
2. Trang thiết bị y tế chẩn đoán in vitro (In vitro diagnostic medical device) gồm thuốc thử, chất hiệu chuẩn, vật liệu kiểm soát, dụng cụ, máy, thiết bị hoặc hệ thống và các sản phẩm khác tham gia hoặc hỗ trợ quá trình thực hiện xét nghiệm được sử dụng riêng rẽ hoặc kết hợp theo chỉ định của chủ sở hữu để phục vụ cho việc kiểm tra các mẫu vật có nguồn gốc từ cơ thể con người.
3. Trang thiết bị y tế đặc thù cá nhân là trang thiết bị y tế được sản xuất đặc biệt theo chỉ định của bác sỹ, có đặc điểm thiết kế riêng biệt sử dụng duy nhất cho một cá nhân cụ thể.
4. Phụ kiện là một sản phẩm được chủ sở hữu TTBYT chỉ định dùng cho mục đích cụ thể cùng với một thiết bị y tế cụ thể nhằm tạo điều kiện hoặc hỗ trợ thiết bị đó sử dụng đúng với mục đích dự định của nó.
5. Chủ sở hữu TTBYT (Product owner) gồm tổ chức, cá nhân thực hiện việc:
- Cung cấp trang thiết bị y tế bằng tên riêng của mình hoặc bằng bất kỳ nhãn hiệu, thiết kế, tên thương mại hoặc tên khác hoặc mã hiệu khác thuộc sở hữu hay kiểm soát của cá nhân, tổ chức đó;
- Chịu trách nhiệm về việc thiết kế, sản xuất, lắp ráp, xử lý, nhãn mác, bao bì hoặc sửa chữa trang thiết bị y tế hoặc xác định mục đích sử dụng của trang thiết bị y tế đó.
Điều 3: Nguyên tắc quản lý trang thiết bị y tế
- Bảo đảm chất lượng, an toàn và sử dụng hiệu quả TTBYT.
- Thông tin đầy đủ, chính xác, kịp thời về đặc tính kỹ thuật, công dụng của TTBYT và các yếu tố nguy cơ có thể xảy ra đối với người sử dụng.
- Bảo đảm truy xuất nguồn gốc của TTBYT.
- Quản lý TTBYT phải dựa trên phân loại về mức độ rủi ro và tiêu chuẩn quốc gia, quy chuẩn kỹ thuật quốc gia tương ứng do cơ quan quản lý nhà nước có thẩm quyền ban hành, thừa nhận hoặc do tổ chức, cá nhân công bố áp dụng theo quy định của pháp luật.
- TTBYT là phương tiện đo, thiết bị bức xạ phải được quản lý theo quy định của pháp luật về đo lường, pháp luật về năng lượng nguyên tử và quy định tại Nghị định này.
- Hóa chất, chế phẩm chỉ có một mục đích là khử khuẩn TTBYT được quản lý theo quy định của Nghị định này. Hóa chất, chế phẩm có mục đích khử khuẩn trang thiết bị y tế nhưng ngoài ra còn có mục đích sử dụng khác được quản lý theo quy định của pháp luật về hóa chất, chế phẩm diệt côn trùng, diệt khuẩn dùng trong lĩnh vực gia dụng và y tế.
- TTBYT, nguyên liệu sản xuất TTBYT và chất ngoại kiểm có chứa chất ma túy và tiền chất phải được quản lý xuất nhập khẩu theo quy định của pháp luật về phòng, chống ma túy và quản lý theo quy định tại Nghị định này.
- Không áp dụng các quy định về phân loại, cấp số lưu hành, công bố đủ điều kiện mua bán của Nghị định này đối với:
- Phần mềm (software) sử dụng cho trang thiết bị y tế;
- TTBYT được mua bán như hàng hóa thông thường nhập khẩu theo hình thức quà tặng, quà biếu cho cá nhân hoặc tổ chức không phải là cơ sở y tế.
Loại, nguyên tắc phân loại trang thiết bị y tế
- TTBYT được phân làm 4 loại dựa trên mức độ rủi ro tiềm ẩn liên quan đến thiết kế kỹ thuật và sản xuất các TTBYT đó:
- TTBYT thuộc loại A là TTBYT có mức độ rủi ro thấp.
- TTBYT thuộc loại B, C, D: có mức độ rủi ro trung bình thấp đến rủi ro
- Nguyên tắc phân loại trang thiết bị y tế:
- Việc phân loại TTBYT phải dựa trên cơ sở quy tắc phân loại về mức độ rủi
- TTBYT chỉ có một mục đích sử dụng nhưng mục đích sử dụng đó có thể được phân loại vào hai hoặc nhiều mức độ rủi ro khác nhau thì áp dụng việc phân loại theo mức độ rủi ro cao nhất.
- TTBYT có nhiều mục đích sử dụng và mỗi mục đích sử dụng có mức độ rủi ro khác nhau thì áp dụng việc phân loại theo mức độ rủi ro cao nhất.
- Trong trường hợp TTBYT được thiết kế để sử dụng kết hợp với một TTBYTkhác thì mỗi TTBYT phải được phân loại mức độ rủi ro riêng biệt.
Trường hợp đối với TTBYT chẩn đoán in vitro là thiết bị, hệ thống thiết bị có tham gia vào quá trình xét nghiệm và các thuốc thử, chất chứng, chất chuẩn, chất hiệu chuẩn, vật liệu kiểm soát được phân loại mức độ rủi ro riêng biệt nhưng kết quả phân loại phải căn cứ vào mức độ rủi ro cao nhất của mục đích sử dụng cuối cùng của tổng thể trang thiết bị y tế kết hợp đó. Các TTBYT chẩn đoán in vitro là các sản phẩm khác tham gia hoặc hỗ trợ quá trình thực hiện xét nghiệm được phân loại mức độ rủi ro riêng biệt.
*Lưu ý: Việc phân loại TTBYT phải được thực hiện bởi cơ sở phân loại là cơ sở đứng tên công bố tiêu chuẩn áp dụng hoặc đăng ký lưu hành.
Sản xuất trang thiết bị y tế
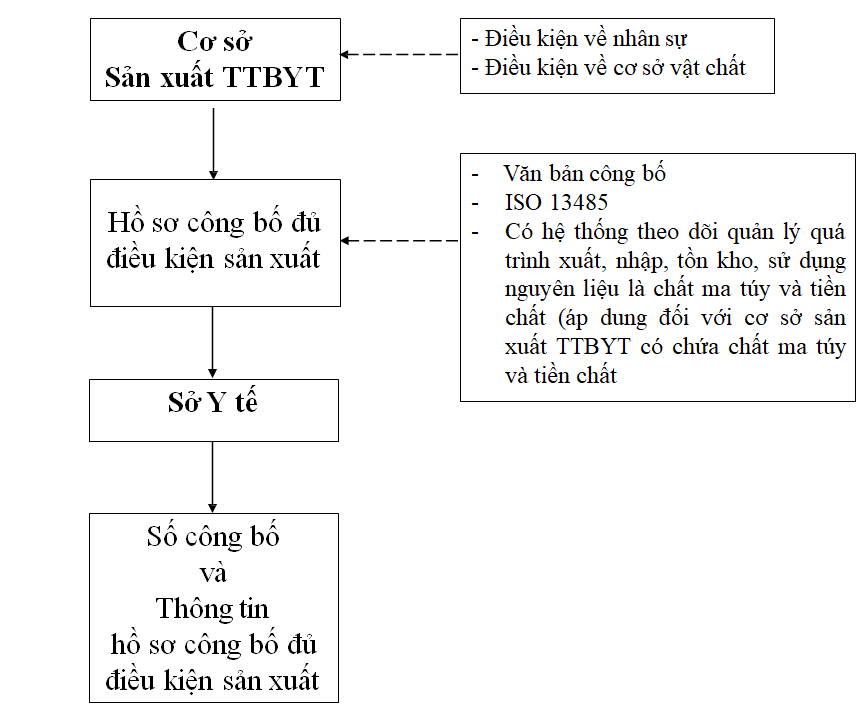
Công bố tiêu chuẩn áp dụng
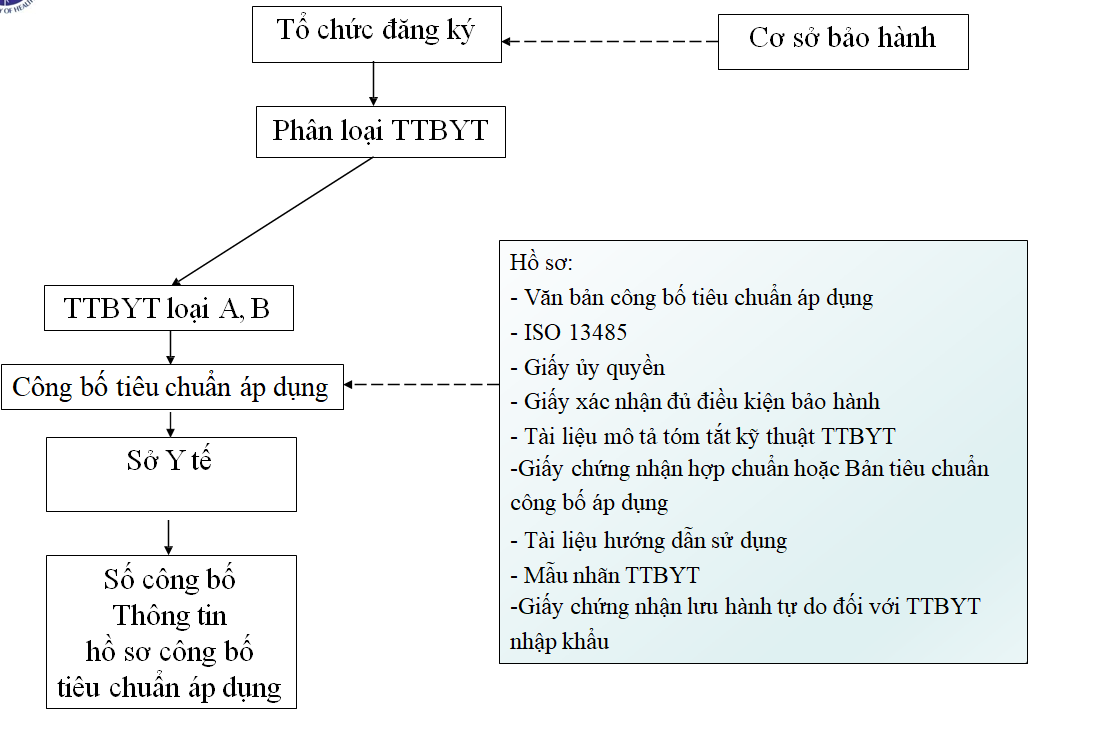
Đăng ký lưu hành trang thiết bị y tế
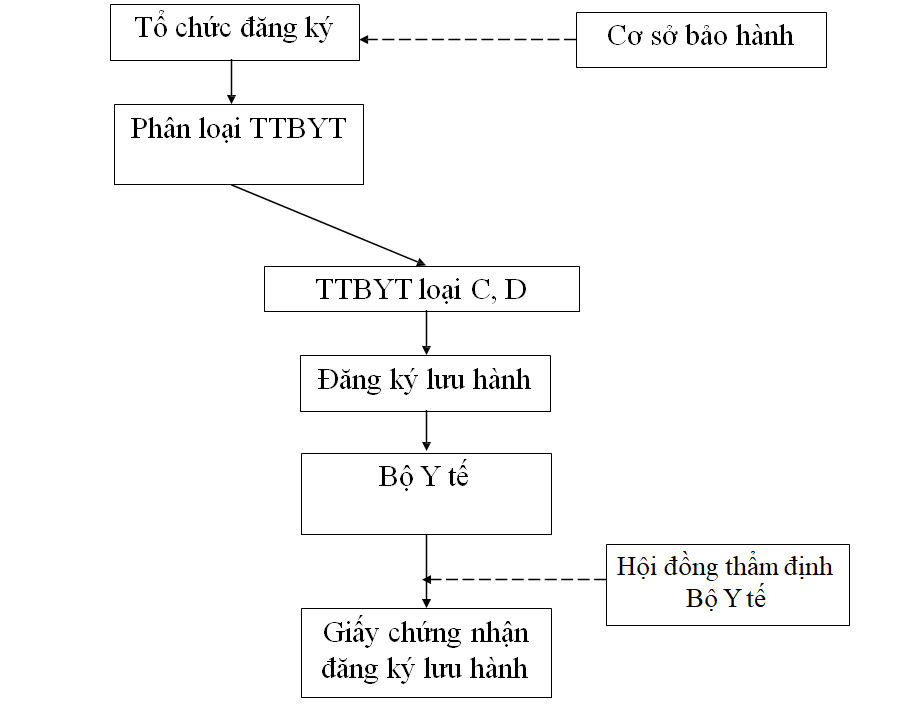
Hồ sơ đề nghị cấp giấy chứng nhận đăng ký lưu hành
|
STT |
Tên giấy tờ | QCVN | Phương
tiện đo |
Cấp
nhanh |
Cấp
khẩn cấp |
Khác |
| 1 | ISO 13485 | X | X | |||
| 2 | Giấy ủy quyền | X | X | |||
| 3 | Giấy xác nhận đủ điều kiện bảo hành | X | X | |||
| 4 | Giấy lưu hành đối với trang thiết bị y tế nhập khẩu | X | X | |||
| 5 | Giấy lưu hành được cấp bởi một trong các nước tham
chiếu |
X | ||||
| 6 | Giấy lưu hành đối với trang thiết bị y tế nhập khẩu và
Giấy phép nhập khẩu hoặc Số lưu hành hoặc Giấy chứng nhận đăng ký lưu hành |
X | ||||
| 7 | Giấy chứng nhận đánh giá chất lượng đối với TTBYT
chẩn đoán in vitro |
X | x | |||
| 8 | Giấy lưu hành hoặc giấy phép sử dụng trong trường hợp
khẩn cấp đối với TTBYT nhập khẩu. |
X | ||||
| 9 | Hợp đồng chuyển giao công nghệ | X | ||||
| 10 | Hợp đồng gia công | X | ||||
| 11 | Hồ sơ CSDT | X | X | X | X | X |
| 12 | Kết quả thẩm định hồ sơ CSDT của đơn vị do Bộ trưởng
Bộ Y tế chỉ định kèm theo hồ sơ CSDT |
X | ||||
| 13 | Giấy chứng nhận hợp quy | X | ||||
|
14 |
Quyết định phê duyệt mẫu |
X |
Cấp nhanh số lưu hành mới đối với trang thiết bị y tế
a) Đã được một trong các tổ chức hoặc nước sau cấp giấy chứng nhận lưu hành tự do (Certificate of Free Sale) hoặc giấy chứng nhận lưu hành (Market Authorization):
- Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) – Mỹ;
- Cục Quản lý hàng hóa trị liệu (TGA) – Úc;
- Cơ quan quản lý y tế Canada (Health Canada);
- Bộ Y tế, Lao động và Phúc lợi Nhật Bản (MHLW) hoặc Cơ quan Dược phẩm và Thiết bị y tế (PMDA) – Nhật Bản, các nước thành viên EU, Anh, Thụy Sỹ;
- Cục Quản lý sản phẩm y tế quốc gia cấp trung ương (National Medical Products Administration – NMPA) – Trung Quốc;
- Bộ An toàn thực phẩm và dược phẩm (Ministry of Food & Drug Safety – MFDS) – Hàn Quốc hoặc thuộc danh sách các tổ chức cấp giấy lưu hành được cơ quan có thẩm quyền của Việt Nam công nhận;
b) Đã được cấp Giấy phép nhập khẩu hoặc Số lưu hành hoặc Giấy chứng nhận đăng ký lưu hành theo hình thức thương mại tại Việt Nam, trừ các trường hợp đã bị thu hồi trước ngày Nghị định này có hiệu lực;
Cấp khẩn cấp số lưu hành
a) Đã được một trong các nước tham chiếu cho phép lưu hành hoặc sử dụng khẩn cấp;
b)Thuộc danh mục sản phẩm được sử dụng khẩn cấp do Tổ chức Y tế thế giới (WHO) công bố;
c) Thuộc danh mục các sản phẩm phổ biến do Ủy ban an ninh y tế của Châu Âu (Health Security Committee – EUHSC) công bố;
d)Đã được cấp số lưu hành hoặc cấp giấy phép nhập khẩu theo hình thức thương mại tại Việt Nam, trừ các trường hợp đã bị thu hồi trước ngày Nghị định này có hiệu lực;
đ) Được sản xuất trong nước theo hình thức chuyển giao công nghệ đối với trang thiết bị y tế thuộc một trong các trường hợp quy định tại điểm a, b, c hoặc d khoản này;
e) Được sản xuất trong nước theo hình thức gia công đối với trang thiết bị y tế thuộc một trong các trường hợp quy định tại điểm a, b, c hoặc d khoản này.
Cấp số lưu hành trang thiết bị y tế
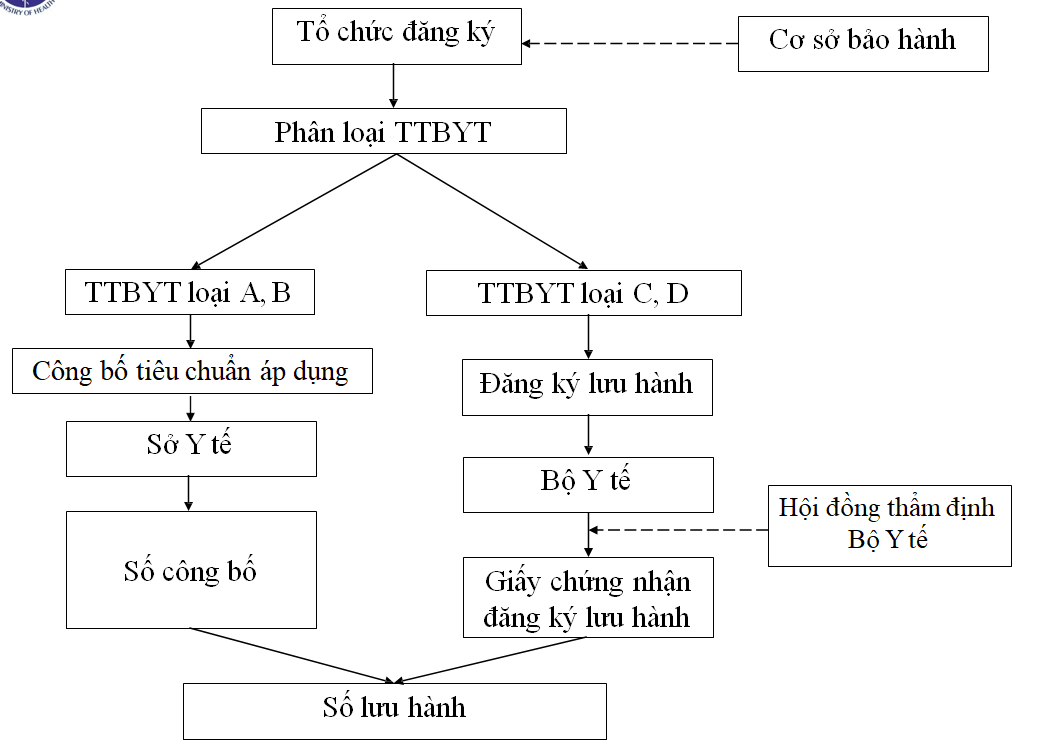
Xuất nhập khẩu trang thiết bị y tế
Điều 46. Nguyên tắc quản lý xuất khẩu, nhập khẩu trang thiết bị y tế
- Tổ chức, cá nhân thực hiện việc xuất khẩu, nhập khẩu TTBYT phải đáp ứng các điều kiện theo quy định của pháp luật về xuất khẩu, nhập khẩu và phải chịu trách nhiệm bảo đảm chất lượng của TTBYT mà mình xuất khẩu, nhập khẩu.
- TTBYT đã có số lưu hành tại Việt Nam được xuất khẩu, nhập khẩu theo nhu cầu, không hạn chế số lượng và không phải qua Bộ Y tế phê duyệt, trừ trang thiết bị y tế có chứa chất ma túy và tiền chất.
- Việc cấp giấy chứng nhận lưu hành tự do chỉ áp dụng đối với TTBYT xuất khẩu theo quy định của Thủ tướng Chính phủ.
- Việc tạm nhập tái xuất, tạm xuất tái nhập hoặc chuyển khẩu, quá cảnh TTBYT thực hiện theo quy định của pháp luật.
- Việc nhập khẩu TTBYT đã qua sử dụng thực hiện theo quy định của pháp luật.
Điều 48. Giấy phép nhập khẩu
Các trường hợp TTBYT phải có giấy phép nhập khẩu:
a) TTBYT chưa có số lưu hành nhập khẩu chỉ để phục vụ nghiên cứu khoa học, kiểm định, kiểm nghiệm, khảo nghiệm, đánh giá chất lượng hoặc đào tạo hướng dẫn việc sử dụng, hướng dẫn sửa chữa TTBYT;
b) TTBYT chưa có số lưu hành nhập khẩu đáp ứng nhu cầu cấp bách phòng, chống dịch bệnh, khắc phục hậu quả thiên tai, thảm họa;
c) TTBYT chưa có số lưu hành nhập khẩu để phục vụ mục đích viện trợ, viện trợ nhân đạo; quà tặng, quà biếu cho cơ sở y tế; phục vụ hội chợ, triển lãm, trưng bày hoặc giới thiệu sản phẩm;
d)TTBYT chưa có số lưu hành nhập khẩu để phục vụ hoạt động khám bệnh, chữa bệnh nhân đạo;
đ) TTBYT chưa có số lưu hành nhập khẩu để sử dụng cho mục đích chữa bệnh cá nhân bao gồm TTBYT đặc thù cá nhân hoặc theo nhu cầu chẩn đoán đặc biệt của cơ sở y tế;
e) TTBYT đã qua sử dụng:
- Nhập khẩu để phục vụ mục đích nghiên cứu, đào tạo (không thực hành trên người và không sử dụng các TTBYT này cho mục đích chẩn đoán, điều trị);
- Tạm nhập, tái xuất để trưng bày, giới thiệu, tham gia hội chợ, triển lãm thương mại.
Mua bán trang thiết bị y tế loại B, C, D
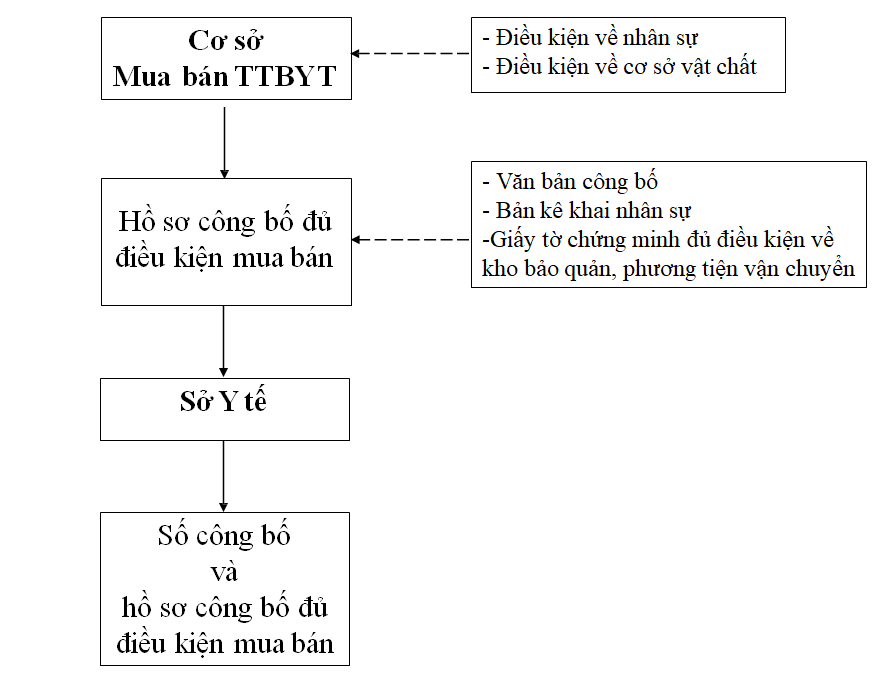
Quản lý giá trang thiết bị y tế
Điều 43. Nguyên tắc quản lý nhà nước về giá trang thiết bị y tế
- Quản lý giá trang thiết bị y tế theo cơ chế thị trường, tôn trọng quyền tự định giá, cạnh tranh về giá của tổ chức, cá nhân kinh doanh trang thiết bị y tế theo quy định của pháp luật.
- Bảo đảm công khai, minh bạch giá trang thiết bị y tế khi lưu hành trên thị trường.
- Bảo vệ quyền, lợi ích hợp pháp của tổ chức, cá nhân kinh doanh, sử dụng và lợi ích của Nhà nước.
- Thực hiện các biện pháp để quản lý giá trang thiết bị y tế phù hợp với điều kiện phát triển kinh tế – xã hội trong từng thời kỳ.
Điều 44. Biện pháp quản lý giá trang thiết bị y tế
- Kê khai giá trang thiết bị y tế trước khi lưu hành tại Việt Nam và cập nhật khi thay đổi giá trang thiết bị y tế đã kê khai theo các quy định tại Nghị định này.
- Niêm yết giá bán buôn, bán lẻ trang thiết bị y tế bằng đồng Việt Nam tại nơi giao dịch hoặc nơi bán trang thiết bị y tế của cơ sở kinh doanh trang thiết bị y tế; thông báo công khai trên bảng, trên giấy hoặc bằng các hình thức khác.
- Công khai giá trúng thầu trang thiết bị y tế của các cơ sở y tế công lập.
- Không được mua bán trang thiết bị y tế khi chưa có giá kê khai và không được mua bán cao hơn giá kê khai trên Cổng thông tin điện tử của Bộ Y tế tại thời điểm mua bán.
Điều 45. Nội dung, trách nhiệm kê khai giá trang thiết bị y tế
| STT | Thông tin | Kê khai | Công khai |
| 1 | Tên, chủng loại trang thiết bị y tế | X | X |
| 2 | Hãng, nước sản xuất; hãng, nước chủ sở hữu | X | X |
| 3 | Đơn vị tính | X | X |
| 4 | Giá vốn nhập khẩu đối với trang thiết bị y tế nhập
khẩu hoặc chi phí sản xuất đối với trang thiết bị y tế sản xuất trong nước |
X | |
| 5 | Lợi nhuận dự kiến | X | |
| 6 | Giá bán tối đa của trang thiết bị y tế tương ứng
với từng cấu hình, tính năng kỹ thuật theo đơn vị tính |
X | X |
| 7 | Giá linh kiện, phụ kiện (nếu có); | X | X |
| 8 | Chi phí bảo hành, bảo dưỡng, bảo trì (nếu có); | X | X |
| 9 | Chi phí đào tạo (nếu có); | X | X |
| 10 | Các chi phí khác (nếu có); | X | X |
- Chủ sở hữu số lưu hành trang thiết bị y tế chịu trách nhiệm:
- Thực hiện việc kê khai giá bao gồm đầy đủ các thông tin quy định tại khoản 1 Điều này và đăng tải thông tin trên Cổng điện tử của Bộ Y tế trước khi đưa trang thiết bị y tế đầu tiên lưu hành trên thị trường Việt Nam;
- Cập nhật giá trang thiết bị y tế khi có thay đổi;
- Chỉ định nhà phân phối thực hiện các quy định tại điểm a và b Điều này đối với trường hợp quy định tại điểm c khoản 1 Điều 25 Nghị định này. Trường hợp có nhiều nhà phân phối cùng thực hiện việc phân phối một mặt hàng, chủ sở hữu số lưu hành trang thiết bị y tế phải chỉ định một nhà phân phối thực hiện việc kê khai giá. Các nhà phân phối khác không phải thực hiện việc kê khai giá nhưng không được bán cao hơn giá do nhà phân phối được chỉ định kê khai;
- Thực hiện việc kê khai, giải trình các yếu tố cấu thành giá với cơ quan quản lý thuế hoặc khi cơ quan quản lý nhà nước có yêu cầu.
- Giá công khai trên Cổng điện tử của Bộ Y tế bao gồm đầy đủ các thông tin quy định tại khoản 2 Điều này.
Tư vấn kỹ thuật về trang thiết bị y tế
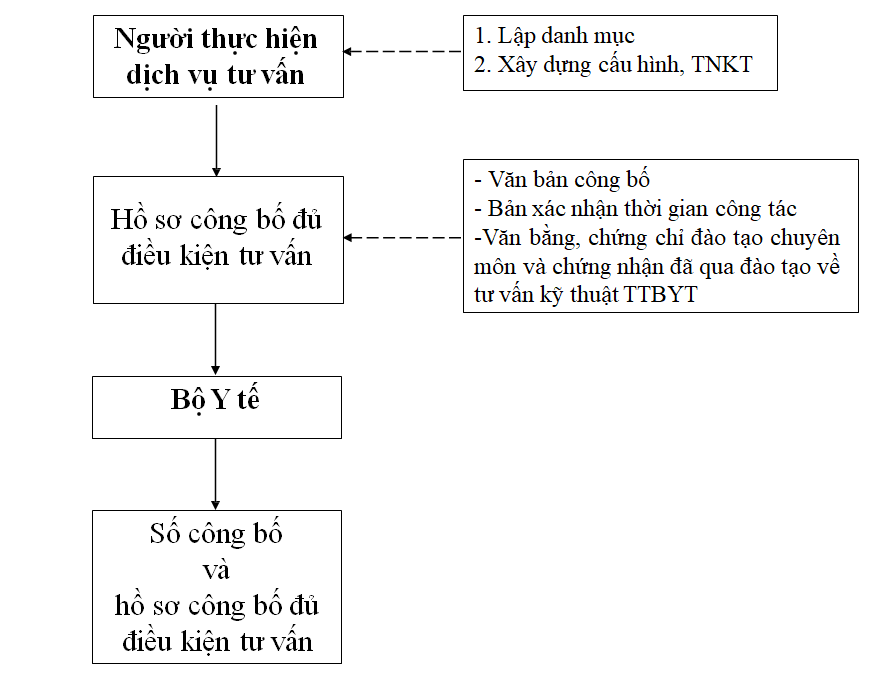
Kiểm định, hiệu chuẩn trang thiết bị y tế
Điều 55. Nguyên tắc kiểm định, hiệu chuẩn TTBYT
1.TTBYT thuộc danh mục do Bộ trưởng Bộ Y tế công bố phải kiểm định về an toàn và tính năng kỹ thuật trước khi đưa vào sử dụng (trừ trường hợp quy định tại Điều 57 Nghị định này), định kỳ, sau sửa chữa lớn. Việc kiểm định TTBYT là phương tiện đo, thiết bị bức xạ thực hiện theo quy định tại khoản 2 Điều này.
2. TTBYT là phương tiện đo hoặc thiết bị bức xạ phải thực hiện kiểm định, hiệu chuẩn theo quy định của pháp luật về đo lường và năng lượng nguyên tử.
Điều 50. Điều kiện kinh doanh dịch vụ kiểm định TTBYT
Điều kiện về cơ sở vật chất, nhân sự; hồ sơ đề nghị cấp Giấy chứng nhận; hình thức nộp hồ sơ; trình tự cấp mới, cấp bổ sung, cấp lại và thu hồi Giấy chứng nhận đăng ký hoạt động kiểm định TTBYT được thực hiện theo quy định của pháp luật hiện hành về điều kiện kinh doanh dịch vụ đánh giá sự phù hợp;
Trong đó, việc đáp ứng yêu cầu chuyên môn đối với lĩnh vực kiểm định TTBYT được quy định như sau: mỗi quy trình kiểm định mà tổ chức kiểm định đăng ký thực hiện phải có tối thiểu 02 kiểm định viên có chứng nhận đã qua đào tạo về quy trình kiểm định đó.
Quản lý nguyên liệu sản xuất trang thiết bị y tế, chất ngoại kiểm chứa chất ma tuý và tiền chất
Điều 59. Nguyên tắc quản lý nguyên liệu sản xuất trang thiết bị y tế, chất ngoại kiểm chứa chất ma túy và tiền chất
1.Nguyên liệu sản xuất trang thiết bị y tế, chất ngoại kiểm chứa chất ma túy và tiền chất phải công bố nồng độ, hàm lượng trước khi thực hiện xuất khẩu, nhập khẩu tại Việt Nam.
2.Việc thông quan phải căn cứ theo số công bố và không cần giấy phép nhập khẩu của Bộ Y tế.
Điều 60. Hồ sơ, thủ tục công bố đối với nguyên liệu sản xuất trang thiết bị y tế, chất ngoại kiểm chứa chất ma túy và tiền chất
- Hồ sơ công bố:
a) Văn bản công bố nguyên liệu sản xuất trang thiết bị y tế, chất ngoại kiểm có chứa chất ma túy và tiền chất;
b) Giấy chứng nhận quản lý chất lượng;
c) Tài liệu kỹ thuật.
- Thủ tục công bố nồng độ, hàm lượng ma túy và tiền chất:
a) Trước khi thực hiện nhập khẩu nguyên liệu sản xuất trang thiết bị y tế và chất ngoại kiểm có chứa chất ma túy và tiền chất, cơ sở nhập khẩu có trách nhiệm đăng tải hồ sơ công bố đầy đủ, hợp lệ theo quy định tại khoản 1 Điều này trên Cổng thông tin điện tử về quản lý trang thiết bị y tế;
b) Sau khi nhận được hồ sơ đầy đủ, hợp lệ, Bộ Y tế đăng tải công khai trên Cổng thông tin điện tử về quản lý trang thiết bị y tế các thông tin và hồ sơ công bố đối với nguyên liệu sản xuất trang thiết bị y tế và chất ngoại kiểm có chứa chất ma túy và tiền chất.
- Cơ sở nhập khẩu, xuất khẩu có trách nhiệm thực hiện lại việc công bố nồng độ, hàm lượng ma túy và tiền chất khi có bất kỳ thay đổi trong hồ sơ đã công bố.
Quảng cáo trang thiết bị y tế
Điều 62. Quảng cáo trang thiết bị y tế
1. Nội dung quảng cáo TTBYT phải phù hợp với một trong các tài liệu sau đây:
a) Hồ sơ công bố tiêu chuẩn áp dụng đối với TTBYT thuộc loại A, B;
b) Hồ sơ đăng ký lưu hành đối với TTBYT thuộc loại C, D.
2. Quảng cáo TTBYT phải có các nội dung sau đây:
a) Tên TTBYT, chủng loại, mã sản phẩm, hãng sản xuất, nước sản xuất;
b) Số lưu hành;
c) Tính năng, tác dụng;
d) Tên, địa chỉ của chủ sở hữu số lưu hành TTBYT hoặc tổ chức được chủ sở hữu số lưu hành trang thiết bị y tế ủy quyền;
đ) Cảnh báo liên quan đến sức khỏe người sử dụng, điều kiện bảo quản (nếu có).
3. Quảng cáo TTBYT trên báo nói, báo hình phải đọc hoặc thể hiện rõ ràng nội dung quy định tại khoản 2 Điều này.
4. Trước khi thực hiện quảng cáo, chủ sở hữu số lưu hành TTBYT hoặc tổ chức được chủ sở hữu số lưu hành trang thiết bị y tế ủy quyền bằng văn bản có trách nhiệm đăng tải công khai trên Cổng thông tin điện tử về quản lý trang thiết bị y tế nội dung và hình thức dự kiến quảng cáo.
Điều khoản chuyển tiếp
a) TTBYT đã được cấp số lưu hành theo quy định của Nghị định số 36/2016/NĐ-CP thì số lưu hành này có giá trị không thời hạn;
b) TTBYT sản xuất trong nước đã được cấp giấy chứng nhận đăng ký lưu hành thì giấy chứng nhận đăng ký lưu hành có giá trị sử dụng đến hết thời gian ghi trên giấy chứng nhận đăng ký lưu hành;
c) TTBYT không phải là sinh phẩm chẩn đoán in vitro đã được cấp giấy phép nhập khẩu từ ngày 01//01/ 2018 thì giấy phép nhập khẩu có hiệu lực đến hết ngày 31/12/2022;
d) Đối với TTBYT không thuộc danh mục phải cấp giấy phép nhập khẩu (trừ hóa chất, chế phẩm diệt côn trùng, diệt khuẩn dùng trong lĩnh vực gia dụng và y tế chỉ có một mục đích là khử khuẩn TTBYT) và đã có bản phân loại là trang thiết bị y tế thuộc loại C, D được Bộ Y tế công bố thông tin trên Cổng thông tin điện tử được tiếp tục nhập khẩu đến hết ngày 31/12/2022 theo nhu cầu, không hạn chế số lượng mà không cần văn bản xác nhận là TTBYT của Bộ Y tế khi thực hiện thủ tục thông quan;
đ) TTTBYT là sinh phẩm chẩn đoán in vitro đã được cấp số đăng ký lưu hành từ ngày 01/01/2014 đến ngày 31/12/2017 thì số đăng ký lưu hành này có giá trị sử dụng đến hết ngày 31/12/2022;
e)TTTBYT là sinh phẩm chẩn đoán in vitro đã được cấp số đăng ký lưu hành từ ngày 01/01/2018 thì số đăng ký lưu hành này có giá trị sử dụng đến hết thời hạn ghi trên giấy đăng ký lưu hành;
g) TTBYT là sinh phẩm chẩn đoán in vitro nhập khẩu đã được cấp giấy phép nhập khẩu từ ngày 01/01/2018 thì giấy phép nhập khẩu này có giá trị sử dụng đến hết ngày 31/12/2022 và không hạn chế số lượng nhập khẩu. Cơ quan Hải quan không thực hiện việc kiểm soát số lượng nhập khẩu với trường hợp này.
5. Các hồ sơ đề nghị cấp số đăng ký lưu hành đã nộp theo quy định của Nghị định số 36/2016/NĐ- CP trước ngày 01/01/2022 đến thời điểm Nghị định có hiệu lực thi hành chưa được cấp số lưu hành được xử lý như sau:
a) Đối với hồ sơ đăng ký lưu hành của trang thiết bị y tế thuộc loại B, Bộ Y tế hướng dẫn các doanh nghiệp đã nộp hồ sơ tiến hành rà soát để thực hiện việc công bố tiêu chuẩn áp dụng theo quy định tại Nghị định này mà không phải nộp lại phí thẩm định cấp phép lưu hành;
b) Đối với hồ sơ đăng ký lưu hành của trang thiết bị y tế thuộc loại C, D nếu đáp ứng điều kiện quy định tại khoản 3 Điều 30 Nghị định này, Bộ Y tế được cấp số lưu hành theo thủ tục quy định tại Điều 32 Nghị định này;
c) Được sử dụng kết quả phân loại do tổ chức phân loại đã được cấp Phiếu tiếp nhận hồ sơ công bố đủ điều kiện phân loại trang thiết bị y tế trước ngày Nghị định này có hiệu lực thi hành trong hồ sơ đề nghị cấp số lưu hành.
6. Hồ sơ đề nghị cấp giấy phép nhập khẩu đối với trang thiết bị y tế đã nộp hồ sơ trước ngày 01/01/ 2022 thì được tiếp tục giải quyết theo quy định của các văn bản quy phạm pháp luật do Bộ trưởng Bộ Y tế ban hành trước ngày Nghị định này có hiệu lực thi hành. Giấy phép nhập khẩu được cấp theo quy định tại khoản này có giá trị sử dụng đến hết ngày 31/12/ 2022.
7. Công khai nội dung và quảng cáo trang thiết bị y tế bắt đầu áp dụng từ ngày 01/7/2022.
8. Chủ sở hữu số lưu hành hoặc cơ sở đứng tên trong giấy phép nhập khẩu trang thiết bị y tế được cấp trước ngày Nghị định này có hiệu lực thi hành phải thực hiện quy định tại khoản 4 Điều 45 Nghị định này trước ngày 01/4/2022 đối với trang thiết bị y tế đang lưu hành trên thị trường Việt Nam và trước khi đưa trang thiết bị y tế lần đầu tiên lưu hành trên thị trường Việt Nam.
Ứng dụng Công nghệ thông tin trong cải cách thủ tục hành chính, hỗ trợ doanh nghiệp trong hoạt động sản xuất, kinh doanh Trang thiết bị y tế
Các thủ tục thực hiện trực tuyến
1.Công bố đủ điều kiện sản xuất trang thiết bị y tế.
2.Công bố tiêu chuẩn áp dụng trang thiết bị y tế.
3.Đăng ký lưu hành trang thiết bị y tế.
4.Công bố đủ điều kiện mua bán trang thiết bị y tế.
5.Công bố đủ điều kiện tư vấn về kỹ thuật trang thiết bị y tế.
6.Đề nghị cấp giấy chứng nhận đăng ký hoạt động kiểm định trang thiết bị y tế.
7.Đề nghị cấp giấy phép nhập khẩu trang thiết bị y tế.
8.Đề nghị cấp giấy chứng nhận lưu hành tự do cho trang thiết bị y tế sản xuất trong nước.
9.Kê khai giá trang thiết bị y tế.
10.Công bố nồng độ, hàm lượng trong nguyên liệu sản xuất trang thiết bị y tế, chất ngoại kiểm chứa chất ma túy và tiền chất.
11.Công khai nội dung và hình thức quảng cáo trang thiết bị y tế.
Vai trò, trách nhiệm của các bên
Điều 64. Quản lý, sử dụng TTBYT trong các cơ sở y tế của Nhà nước
Các cơ sở y tế của Nhà nước ngoài việc thực hiện các nguyên tắc quản lý, sử dụng TTBYT theo quy định tại Nghị định này, phải thực hiện quản lý TTBYT theo các quy định sau:
1.Việc đầu tư, mua sắm, quản lý, sử dụng trang thiết bị y tế để thực hiện theo quy định của pháp luật về quản lý sử dụng tài sản công.
2.Khuyến khích sử dụng các trang thiết bị y tế sản xuất trong nước.
Điều 65. Quyền và trách nhiệm của cơ sở y tế trong việc quản lý, sử dụng TTBYT
- Cơ sở y tế có quyền:
a) Yêu cầu chủ sở hữu số lưu hành hoặc cơ sở bảo hành được chứng nhận bởi chủ sở hữu TTBYT thực hiện việc bảo dưỡng định kỳ trong thời hạn bảo hành;
b) Yêu cầu bên bán cung cấp tài liệu kỹ thuật của TTBYT;
c) Tiếp nhận các TTBYT đã qua sử dụng phục vụ mục đích nghiên cứu khoa học và hướng dẫn sử dụng, sửa chữa TTBYT.
- Cơ sở y tế có trách nhiệm:
a) Sử dụng, vận hành TTBYT theo đúng hướng dẫn của chủ sở hữu trang thiết bị y tế;
b) Định kỳ bảo dưỡng, kiểm định, hiệu chuẩn theo hướng dẫn của chủ sở hữu TTBYT hoặc quy định của pháp luật;
c) Tham gia thử nghiệm, đánh giá chất lượng TTBYT;
d) Báo cáo về các trường hợp TTBYT có lỗi và các thông tin khác theo yêu cầu của cơ quan nhà nước có thẩm quyền.
Điều 74. Trách nhiệm của tổ chức, cá nhân kinh doanh TTBYT
1.Tổ chức, cá nhân kinh doanh TTBYT phải chịu trách nhiệm về an toàn, chất lượng đối với TTBYT do mình kinh doanh.
2. Cơ sở sản xuất TTBYT trong nước có trách nhiệm quản lý chất lượng TTBYT trong quá trình sản xuất, vận chuyển, bảo quản trang thiết bị y tế theo đúng hồ sơ đã cấp số lưu hành.
3. Chủ sở hữu số lưu hành có trách nhiệm:
a) Thực hiện việc phân loại, công bố trên Cổng thông tin điện tử của Bộ Y tế và chịu trách nhiệm trước pháp luật về kết quả phân loại đối với TTBYT mà mình đã thực hiện phân loại;
Thực hiện các biện pháp khắc phục đối với những trường hợp ban hành kết quả phân loại sai làm giảm mức độ rủi ro của TTBYT hoặc ban hành kết quả phân loại sai về thẩm quyền quy định tại Nghị định này.
b) Thực hiện việc công bố tiêu chuẩn áp dụng hoặc đăng ký lưu hành TTBYT theo quy định của Nghị định này. Chịu trách nhiệm trước pháp luật về tính chính xác, trung thực của hồ sơ đề nghị cấp số lưu hành.
d) Lập, duy trì hồ sơ theo dõi TTBYT và thực hiện truy xuất nguồn gốc TTBYT;
e) Cảnh báo kịp thời, đầy đủ, chính xác về nguy cơ gây ảnh hưởng xấu đến sức khỏe người sử dụng, môi trường;
k) Chịu trách nhiệm bảo đảm các giấy tờ sau luôn có hiệu lực trong thời gian số lưu hành còn giá trị:
-Giấy lưu hành đối với TTBYT nhập khẩu;
-Giấy ủy quyền;
-Giấy xác nhận đủ điều kiện bảo hành.
l) Chịu trách nhiệm bảo đảm TTBYT chỉ được sản xuất trong thời gian giấy chứng nhận đạt tiêu chuẩn quản lý chất lượng của cơ sở sản xuất còn hiệu lực;
m) Chịu trách nhiệm trước pháp luật về tính hợp pháp, chính xác của các tài liệu đã đăng tải khi thực hiện các thủ tục trong Nghị định này;
o) Kê khai, cập nhật giá bán TTBYT hoặc chỉ định một tổ chức thực hiện kê khai, cập nhật giá bán TTBYT;
Một số điểm cần lưu ý
Đề nghị các ban lãnh đạo, các đơn vị quan tâm chỉ đạo đảm bảo an toàn, chất lượng hiệu quả trang thiết bị y tế cho người bệnh và cán bộ nhân viên y tế sử dụng
1.Chỉ đạo nghiên cứu, quán triệt thực hiện các quy định tại Nghị định số 98/2021/NĐ-CP về quản lý TTBYT, Luật đấu thầu số 43/2013/QH13, Thông tư 14/2020/TT-BYT; Chỉ thị số 47/CT-TTg về chấn chỉnh các hoạt động đấu thầu, Chỉ thị 13/CT-TTg về tăng cường sử dụng hàng hóa trong nước sản xuất và các văn bản quy phạm pháp luật liên quan để áp dụng đưa vào hồ sơ thầu các nội dung sau:
- Tính hợp lệ của nhà thầu;
- Tính hợp lệ của sản phẩm;
- Đối với Hồ sơ mời thầu:
- Quy định rõ tiêu chí đánh giá thầu để đảm bảo minh bạch công bằng;
- Quy định rõ trách nhiệm của nhà cung cấp, chủ đầu tư để đảm bảo thiết bị được bàn giao, lắp đặt, hướng dẫn sử dụng, bảo trì đúng quy định chặt chẽ, phát huy hiệu quả đầu tư.
- Quan tâm đến các điều kiện về đào tạo cán bộ sử dụng, bảo dưỡng sửa chữa; chuẩn bị đội ngũ cán bộ chuyên môn, cơ sở hạ tầng kỹ thuật lắp đặt thiết bị để đưa thiết bị vào hoạt động, đáp ứng yêu cầu chuyên môn và phát huy hiệu quả đầu tư, tránh tình trạng đắp chiếu, không sử dụng hoặc hiệu quả sử dụng không cao.
2. Chỉ đạo việc xây dựng và thực hiện nghiêm túc:
- Định mức TTBYT;
- Các quy trình quản lý, khai thác sử dụng, bảo dưỡng, sửa chữa TTBYT đảm bảo chất lượng, an toàn, hiệu quả;
- Có trách nhiệm bố trí kinh phí được trích từ giá dịch vụ kỹ thuật để sử dụng cho công tác bảo trì, bảo dưỡng, sửa chữa, kiểm chuẩn TTBYT ngay từ khi đưa thiết bị vào sử dụng;
- Chủ động trong công tác quản lý và khắc phục sự cố nhằm tăng tuổi thọ cho thiết bị, bảo đảm trang thiết bị luôn trong tình trạng hoạt động tốt.
Nghiên cứu lâm sàng trang thiết bị y tế
Điều 12: Các giai đoạn nghiên cứu lâm sàng trang thiết bị y tế
- Giai đoạn 1: nghiên cứu sơ bộ về tính an toàn và mức độ dễ sử dụng của trang thiết bị y tế đối với bác sĩ và nhân viên y tế.
- Giai đoạn 2: xác định và chứng minh tính an toàn, hiệu quả của trang thiết bị y tế.
- Giai đoạn 3: tiến hành sau khi trang thiết bị y tế đã được lưu hành nhằm tiếp tục nghiên cứu tính an toàn, hiệu quả
Điều 13: Yêu cầu đối với trang thiết bị y tế nghiên cứu lâm sàng
- Đạt tiêu chuẩn chất lượng theo hồ sơ đăng ký nghiên cứu lâm sàng.
- Đã qua kiểm tra, đánh giá các thông số kỹ thuật của thiết bị, đảm bảo chất lượng và an toàn.
- Nhãn trang thiết bị y tế nghiên cứu lâm sàng phải ghi dòng chữ “Trang thiết bị y tế dùng cho nghiên cứu lâm sàng. Cấm dùng cho mục đích khác”. Việc ghi nhãn thực hiện theo quy định của pháp luật về ghi nhãn hàng hóa.
Điều 14: Yêu cầu đối với cơ sở nhận nghiên cứu lâm sàng trang thiết bị y tế
Cơ sở nhận nghiên cứu lâm sàng trang thiết bị y tế phải đáp ứng các yêu cầu sau đây:
- Là cơ sở có chức năng về nghiên cứu khoa học, độc lập đối với tổ chức, cá nhân
- Có trang thiết bị y tế nghiên cứu lâm sàng.
- Có địa điểm, phòng nghiên cứu lâm sàng, hệ thống quản lý chất lượng, tài liệu chuyên môn kỹ thuật đáp ứng nguyên tắc Thực hành lâm sàng tốt.
- Có đủ nhân lực nghiên cứu, trong đó:
+ Nghiên cứu viên chính: có đủ trình độ và năng lực chuyên môn về chuyên ngành nghiên cứu, sử dụng trang thiết bị y tế, có khả năng triển khai nghiên cứu lâm sàng trang thiết bị y tế.
+ Nghiên cứu viên: có đủ trình độ, năng lực chuyên môn phù hợp với yêu cầu nghiên cứu lâm sàng trang thiết bị y tế.
Điều 15: Hồ sơ nghiên cứu lâm sàng trang thiết bị y tế
Hồ sơ nghiên cứu lâm sàng trang thiết bị y tế bao gồm:
+ Hồ sơ đề nghị phê duyệt nghiên cứu lâm sàng trang thiết bị y tế
+ Hồ sơ đề nghị phê duyệt thay đổi nghiên cứu lâm sàng trang thiết bị y tế
+ Hồ sơ đề nghị phê duyệt kết quả nghiên cứu lâm sàng trang thiết bị y tế
1. Hồ sơ đề nghị phê duyệt nghiên cứu lâm sàng trang thiết bị y tế bao gồm:
a. Văn bản đề nghị phê duyệt nghiên cứu lâm sàng trang thiết bị y tế.
b. Hồ sơ thông tin về trang thiết bị y tế nghiên cứu lâm sàng bao gồm:
+ Hồ sơ thông tin sản phẩm nghiên cứu
+Tài liệu nghiên cứu tiền lâm sàng
+ Tài liệu nghiên cứu lâm sàng trang thiết bị y tế các giai đoạn trước
c. Hồ sơ pháp lý của trang thiết bị y tế:
+ Tài liệu kỹ thuật trang thiết bị y tế;
+ Tiêu chuẩn kỹ thuật và phiếu kiểm nghiệm, kiểm định
+ Tờ hướng dẫn sử dụng đã được cấp phép lưu hành đối với các trang thiết bị y tế đề nghị nghiên cứu lâm sàng giai đoạn 3
+ Văn bản xác nhận tham
+ Hợp đồng hợp tác nghiên cứu
d. Đề cương nghiên cứu lâm sàng trang thiết bị y tế và bản thuyết minh bao gồm: Thuyết minh nghiên cứu lâm sàng trang thiết bị y tế và Phiếu thu thập thông tin nghiên cứu hoặc Bệnh án nghiên cứu (Case Report Form – CRF).
đ. Lý lịch khoa học và bản sao giấy chứng nhận hoàn thành khóa học Thực hành tốt nghiên cứu lâm sàng trang thiết bị y tế
e. Bản cung cấp thông tin nghiên cứu và phiếu tình nguyện tham gia nghiên cứu
f. Biên bản thẩm định về khoa học và đạo đức trong nghiên cứu của Hội đồng đạo đức trong nghiên cứu y sinh học cấp cơ sở.
g. Nhãn trang thiết bị theo quy định
2. Hồ sơ đề nghị phê duyệt thay đổi nghiên cứu
- Văn bản đề nghị phê duyệt thay đổi nghiên cứu lâm sàng trang thiết bị y tế.
- Phiên bản cập nhật của các tài liệu tương ứng quy định tại khoản 1 Điều này đã được thay đổi.
- Biên bản thẩm định của Hội đồng đạo đức trong nghiên cứu y sinh học cấp cơ sở đối với những thay đổi nghiên cứu lâm sàng trang thiết bị y tế có ảnh hưởng đến sức khỏe và quyền lợi người tham gia nghiên cứu trang thiết bị y tế hoặc ảnh hưởng đến thiết kế, quy trình và thủ tục nghiên cứu.
3. Hồ sơ đề nghị phê duyệt kết quả nghiên cứu
- Văn bản đề nghị phê duyệt kết quả nghiên cứu.
- Bản sao đề cương nghiên cứu đã được phê duyệt.
- Bản sao Quyết định phê duyệt đề cương nghiên cứu đã được phê duyệt.
- Biên bản thẩm định kết quả nghiên cứu lâm sàng trang thiết bị y tế của hội đồng đạo đức trong nghiên cứu y sinh học cấp cơ sở.
- Báo cáo toàn văn kết quả nghiên cứu lâm sàng trang thiết bị y tế.
4. Yêu cầu đối với hồ sơ
- Hồ sơ nghiên cứu lâm sàng trang thiết bị y tế phải được viết bằng tiếng Việt. Trường hợp không thể hiện bằng tiếng Việt thì phải có thêm bản dịch công chứng của tài liệu đó ra tiếng Việt.
- Đối với các giấy tờ do cơ quan quản lý nước ngoài cấp phải được hợp pháp hoá lãnh sự theo quy định của pháp luật về hợp pháp hóa lãnh sự, trừ trường hợp được miễn theo quy định của pháp luật
Điều 16: Thủ tục, trình tự phê duyệt nghiên cứu lâm sàng
1.Cơ sở nghiên cứu lâm sàng trang thiết bị y tế gửi trực tiếp hoặc qua đường bưu điện 01 bộ hồ sơ đề nghị phê duyệt nghiên cứu lâm sàng trang thiết bị y tế đến Bộ Y tế.
2. Bộ Y tế kiểm tra tính hợp lệ của hồ sơ trong thời hạn 05 ngày làm việc kể từ ngày nhận được hồ sơ.
-Trường hợp hồ sơ hợp lệ trong thời hạn 02 ngày làm việc Bộ Y tế chuyển hồ sơ đến Hội đồng đạo đức trong nghiên cứu y sinh học quốc gia
-Trường hợp hồ sơ không hợp lệ phải có văn bản thông báo, hướng dẫn cụ thể cho cơ sở bổ sung hồ sơ.
3. Trong thời hạn 25 ngày, kể từ ngày nhận đủ hồ sơ hợp lệ, Hội đồng đạo đức quốc gia tổ chức họp và có biên bản thẩm định đề cương nghiên cứu lâm sàng trang thiết bị y tế.
- Trường hợp thẩm định đạt yêu cầu, Hội đồng cấp Giấy chứng nhận chấp thuận đề cương nghiên cứu.
- Trường hợp đề cương nghiên cứu không được chấp thuận hoặc cần sửa chữa, Hội đồng đạo đức quốc gia có văn bản thông báo cho cơ sở nghiên cứu và nêu rõ lý do.
- Trong vòng 07 ngày làm việc kể từ ngày nhận đủ hồ sơ sửa đổi bổ sung, Hội đồng đạo đức quốc gia phải tổ chức họp để xem xét. Trường hợp đạt yêu cầu, Hội đồng cấp Giấy chứng nhận chấp thuận đề cương nghiên cứu.
- Hồ sơ chỉ được xem xét sửa đổi bổ sung tối đa không quá 03 lần.
4. Trong thời hạn 05 ngày làm việc kể từ ngày nhận được Giấy chứng nhận chấp thuận đề cương nghiên cứu và hồ sơ kèm theo, Bộ Y tế quyết định phê duyệt đề cương nghiên cứu lâm sàng trang thiết bị y tế.
Điều 17: Thủ tục, trình tự phê duyệt thay đổi đề cương nghiên cứu
1. Cơ sở nghiên cứu lâm sàng trang thiết bị y tế gửi trực tiếp hoặc qua đường bưu điện 01 bộ hồ sơ đề nghị phê duyệt thay đổi đề cương nghiên cứu lâm sàng trang thiết bị y tế đến Bộ Y tế.
2. Bộ Y tế kiểm tra tính hợp lệ của hồ sơ trong thời hạn 05 ngày làm việc kể từ ngày nhận được hồ sơ. Trường hợp hồ sơ không hợp lệ phải có văn bản thông báo, hướng dẫn cụ thể cho cơ sở bổ sung hồ sơ cho đến khi hồ sơ hợp lệ.
Trường hợp hồ sơ hợp lệ trong thời hạn 02 ngày làm việc Bộ Y tế chuyển hồ sơ đến Hội đồng đạo đức quốc gia để thẩm định và có biên bản thẩm định thay đổi đề cương nghiên cứu lâm sàng trang thiết bị y tế.
3. Trong thời hạn 25 ngày, kể từ ngày nhận đủ hồ sơ hợp lệ, Hội đồng đạo đức quốc gia tổ chức họp Hội đồng và có biên bản thẩm định thay đổi đề cương nghiên cứu lâm sàng trang thiết bị y tế.
- Trường hợp thẩm định đạt yêu cầu, Hội đồng cấp Giấy chứng nhận chấp thuận thay đổi đề cương nghiên cứu
- Trường hợp đề cương nghiên cứu không được chấp thuận hoặc cần sửa chữa, Hội đồng đạo đức quốc gia có văn bản thông báo cho cơ sở nghiên cứu và nêu rõ lý do.
- Trong vòng 07 ngày làm việc kể từ nhận đủ hồ sơ sửa đổi bổ sung, Hội đồng đạo đức quốc gia xem xét.
- Hồ sơ chỉ được xem xét sửa đổi bổ sung tối đa không quá 03 lần.
4. Trong thời hạn 05 ngày làm việc kể từ ngày nhận được Giấy chứng nhận chấp thuận thay đổi đề cương nghiên cứu và hồ sơ kèm theo, Bộ Y tế quyết định phê duyệt thay đổi đề cương nghiên cứu lâm sàng trang thiết bị y tế.
Điều 18: Thủ tục, trình tự phê duyệt kết quả nghiên cứu lâm sàng
1.Cơ sở nghiên cứu lâm sàng trang thiết bị y tế gửi trực tiếp hoặc qua đường bưu điện 01 bộ hồ sơ đề nghị phê duyệt kết quả nghiên cứu lâm sàng trang thiết bị y tế bằng tiếng Việt đến Bộ Y tế.
2.Bộ Y tế kiểm tra tính hợp lệ của hồ sơ trong thời hạn 05 ngày làm việc kể từ ngày nhận được hồ sơ.
+ Trường hợp hồ sơ hợp lệ, trong thời hạn 02 ngày làm việc Bộ Y tế chuyển hồ sơ đến Hội đồng đạo đức quốc gia để thẩm định. Trường hợp hồ sơ không hợp lệ phải có văn bản thông báo, hướng dẫn cụ thể cho cơ sở bổ sung hồ sơ.
+ Cơ sở nghiên cứu lâm sàng trang thiết bị y tế có trách nhiệm hoàn thiện hồ sơ trong thời hạn tối đa 60 ngày kể từ ngày nhận được văn bản thông báo. Quá thời hạn này, thủ tục phê duyệt kết quả nghiên cứu phải thực hiện lại từ đầu.
3. Trong thời hạn 25 ngày, kể từ ngày nhận đủ hồ sơ hợp lệ, Hội đồng đạo đức quốc gia tổ chức họp Hội đồng và có biên bản thẩm định kết quả nghiên cứu trang thiết bị y tế trên lâm sàng.
- Trường hợp thẩm định đạt yêu cầu, Hội đồng có Giấy chứng nhận chấp thuận kết quả nghiên cứu trang thiết bị y tế trên lâm sàng.
- Trường hợp kết quả nghiên cứu không được chấp thuận hoặc cần sửa chữa, Hội đồng đạo đức quốc gia có văn bản thông báo cho cơ sở nghiên cứu và nêu rõ lý do.
- Trong vòng 07 ngày làm việc kể từ nhận đủ hồ sơ sửa đổi bổ sung, Hội đồng đạo đức quốc gia xem xét.
- Hồ sơ chỉ được xem xét sửa đổi bổ sung tối đa không quá 03 lần.
4. Trong thời hạn 05 ngày làm việc kể từ ngày nhận được Giấy chứng nhận chấp thuận kết quả nghiên cứu và hồ sơ kèm theo, Bộ Y tế quyết định phê duyệt kết quả nghiên cứu lâm sàng trang thiết bị y tế.
Điều 19: Trách nhiệm của tổ chức, cá nhân có trang thiết bị y tế
1.Bồi thường thiệt hại cho người tham gia nghiên cứu lâm sàng trang thiết bị y tế nếu có rủi ro xảy ra do nghiên cứu trang thiết bị y tế theo quy định của pháp luật.
2.Ký kết hợp đồng về việc nghiên cứu lâm sàng trang thiết bị y tế với cơ sở nhận nghiên cứu lâm sàng trang thiết bị y tế.
3.Chịu trách nhiệm trước pháp luật về chất lượng và tính an toàn của trang thiết bị y tế do mình cung cấp.
Điều 20: Trách nhiệm của cơ sở nhận nghiên cứu lâm sàng
´1. Chịu trách nhiệm về kết quả nghiên cứu lâm sàng trang thiết bị y tế.
´2. Chịu trách nhiệm về sự an toàn và bảo đảm quyền lợi cho người tham gia nghiên cứu lâm sàng trang thiết bị y tế và bồi thường thiệt hại cho người tham gia nghiên cứu lâm sàng trang thiết bị y tế nếu có rủi ro xảy ra do lỗi của cơ sở nhận nghiên cứu lâm sàng trang thiết bị y tế theo quy định của pháp luật.
´3. Bảo đảm trung thực, khách quan trong nghiên cứu lâm sàng trang thiết bị y tế.
´4. Độc lập về kinh tế, tổ chức nhân sự đối với tổ chức, cá nhân có trang thiết bị y tế nghiên cứu lâm sàng.
Hướng dẫn thực hiện triển khai dịch vụ công trực tuyến (theo nghị định 98/2021/ND-CP)
1. Danh sách thủ tục hành chính
| STT | Thủ tục hành chính |
| 1 | Công bố tiêu chuẩn áp dụng trang thiết bị y tế loại A, B |
| 2 | Công bố đủ điều kiện sản xuất trang thiết bị y tế |
| 3 | Công bố đủ điều kiện mua bán trang thiết bị y tế loại B, C, D |
2. Quy trình chung giải quyết thủ tục hành chính
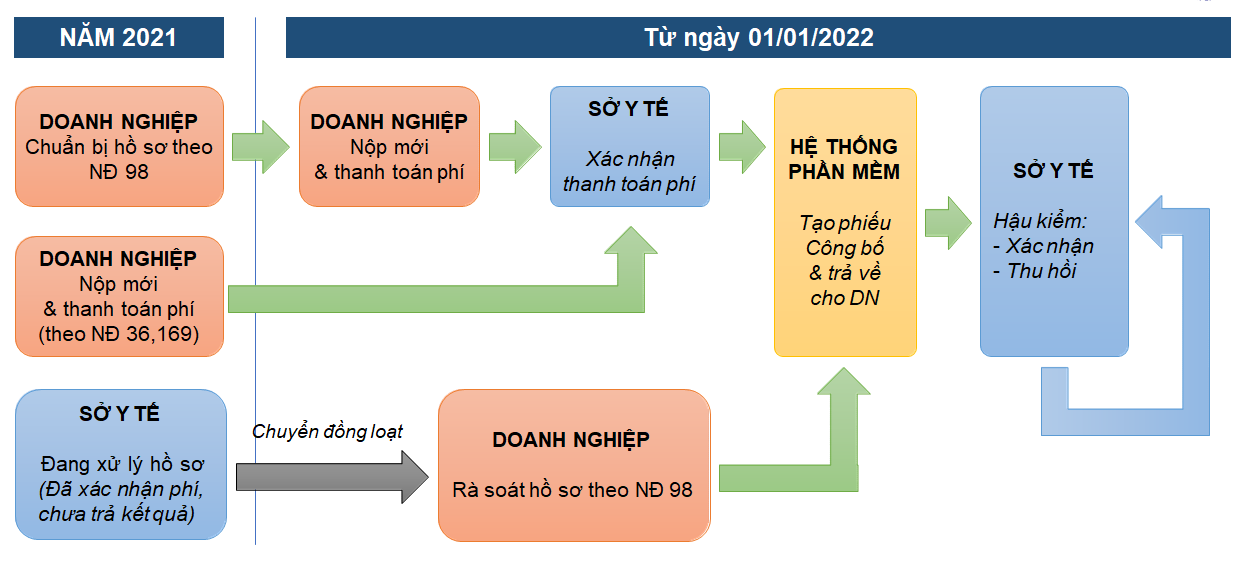
3. Chức năng hậu kiểm – Sở y tế
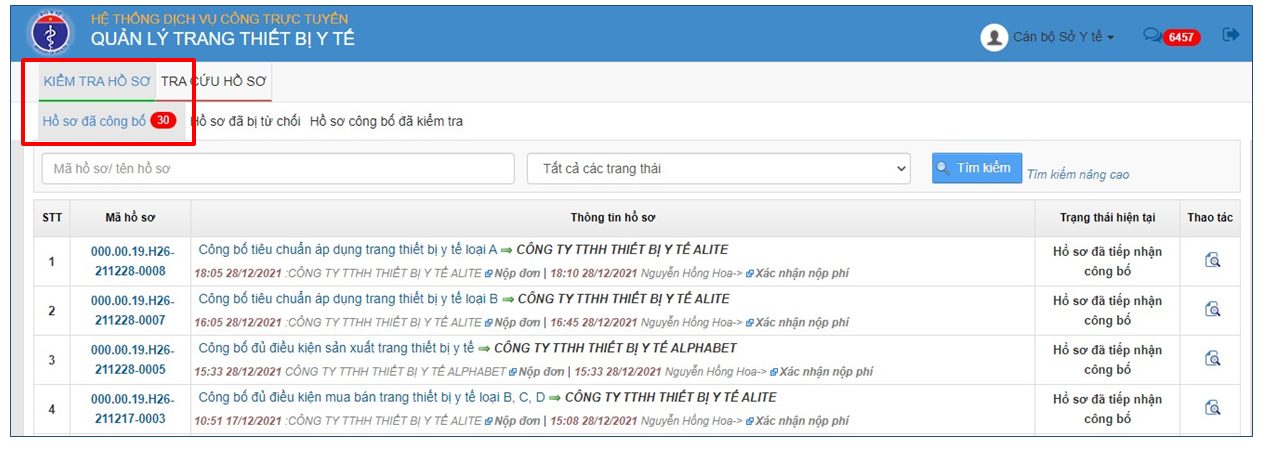
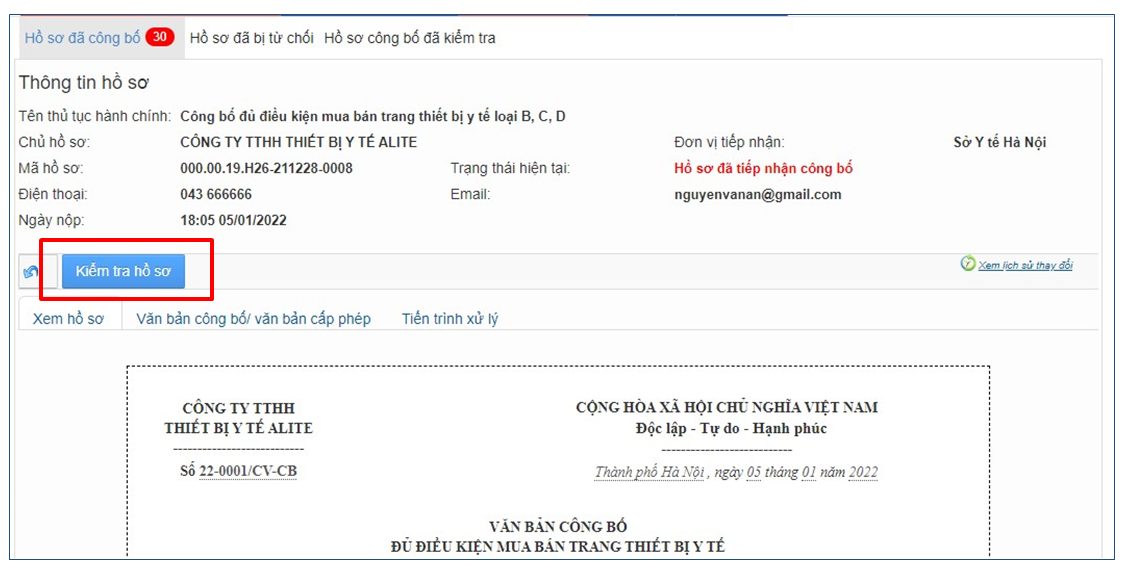
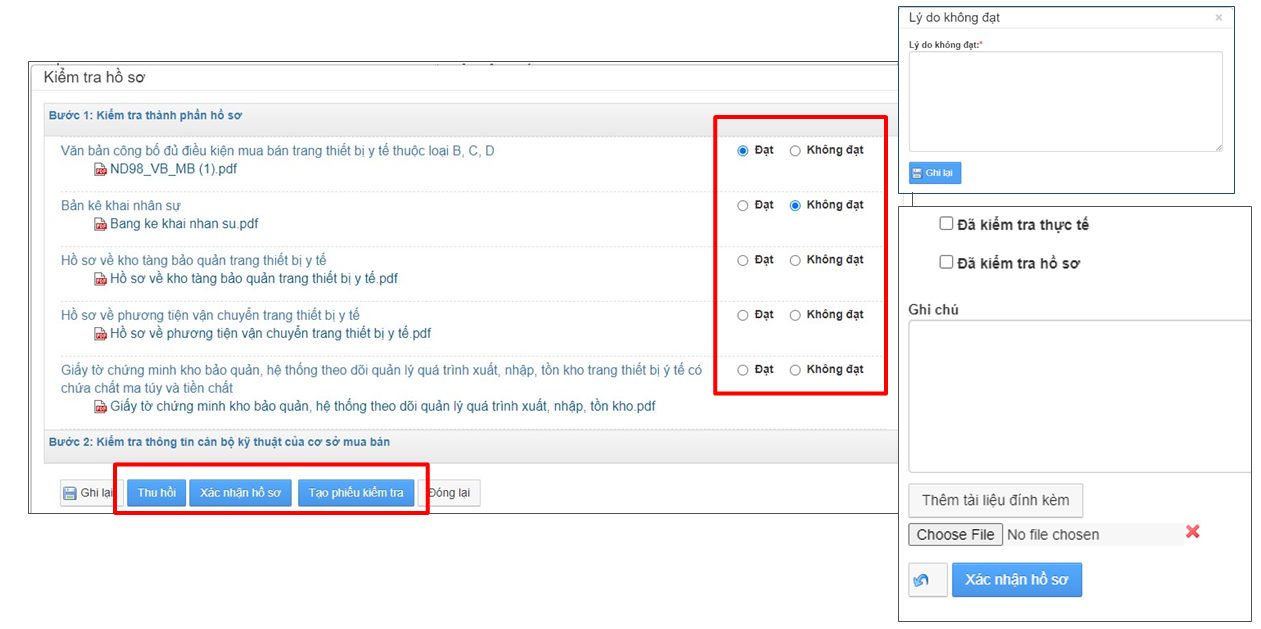
4. Tra cứu văn bản thu hồi
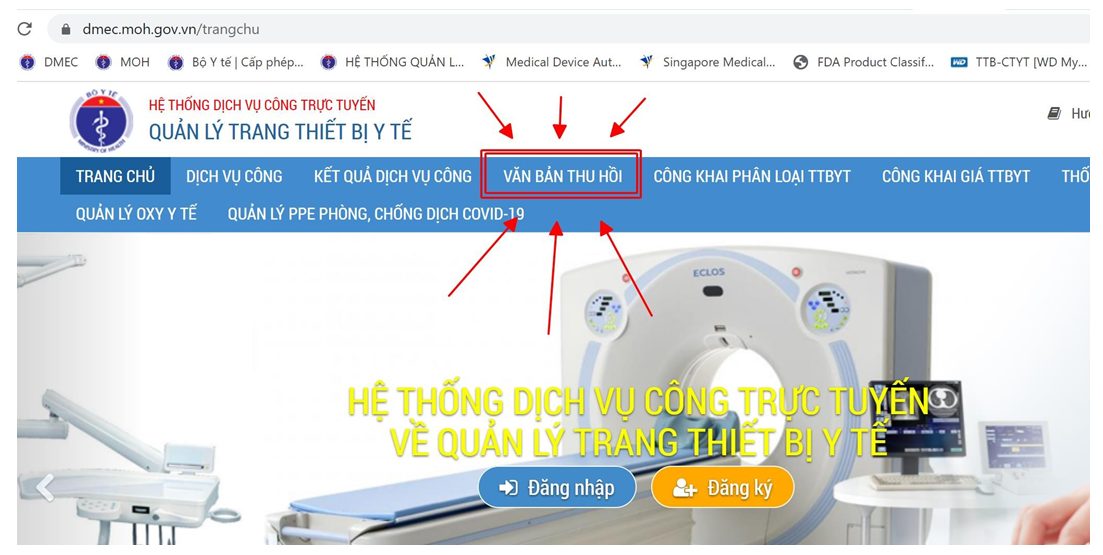
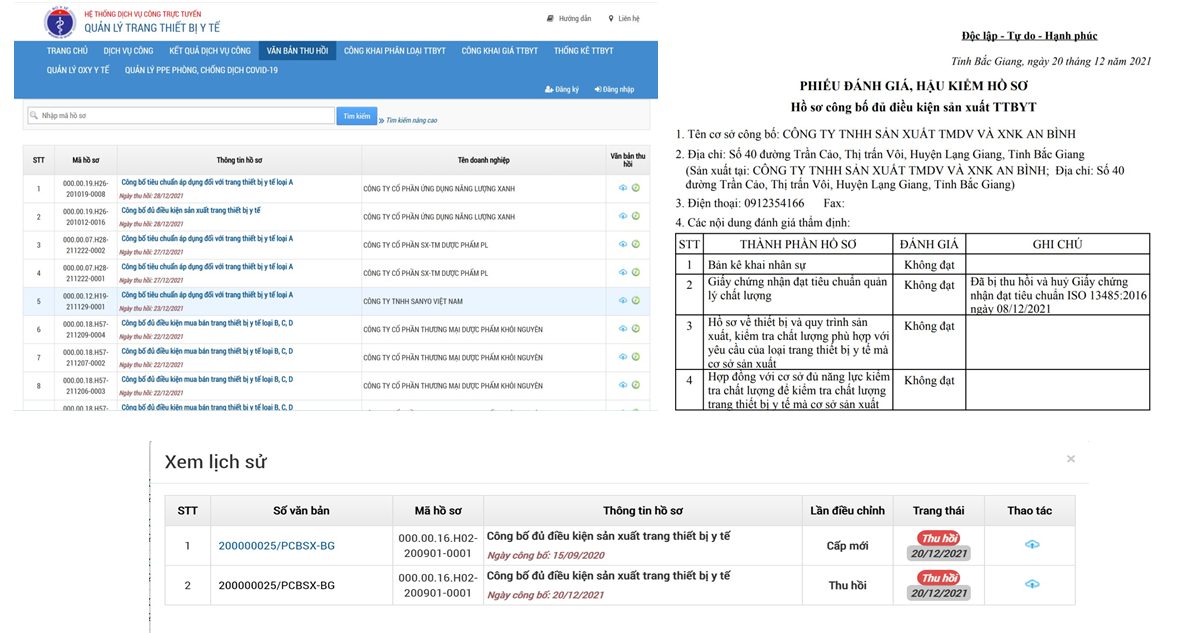
5. Quản trị người dùng tại sở y tế
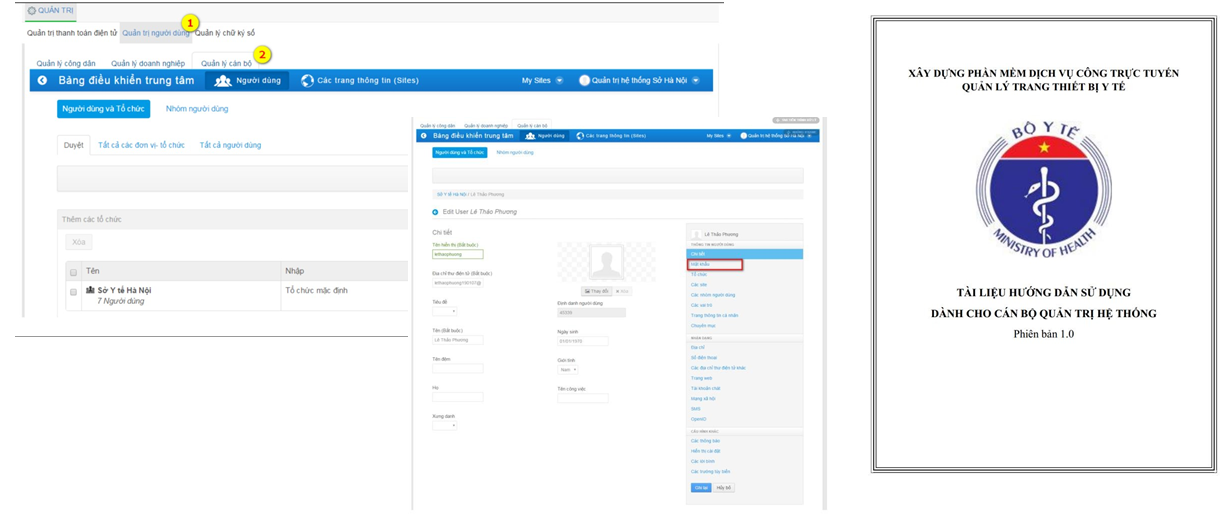
Trên đây là văn bản hướng dẫn nội dung nghị định 98/2021/NĐ-CP về quản lý trang thiết bị y tế mà Sao Mai muốn gửi đến bạn. Nếu bạn có thắc mắc nào hãy liên hệ với chúng tôi để được tư vấn.
Mọi thông tin chi tiết xin vui lòng liên hệ:
CÔNG TY CỔ PHẦN PHÁT TRIỂN QUỐC TẾ SAO MAI
Hotline : +84 924 444 992
Email: info@saomaicorp.com.vn
Địa chỉ: Tầng 10 Tòa nhà Sico, Số 2, Ngõ 2, Đường Nguyễn Hoàng, Quận Nam Từ Liêm, Thành Phố Hà Nội, Việt Nam.