Làm thế nào để đăng ký lưu hành trang thiết bị y tế?
Đăng ký lưu hành trang thiết bị y tế ở đâu?
Đăng ký lưu hành trang thiết bị y tế là sản phẩm khử khuẩn cần lưu ý gì?
Đăng ký lưu hành trang thiết bị y tế mất bao nhiêu thời gian?
Đăng ký lưu hành trang thiết bị y tế cần chuẩn bị giấy tờ gì?
Công ty cổ phần phát triển quốc tế sao mai chúng tôi chuyên cung cấp các dịch vụ liên quan đến đăng ký lưu hành trang thiết bị y tế , công bố trang thiết bị y tế loại A và xin giấy phép nhập khẩu trang thiết bị y tế. Vừa qua có rất nhiều khách hàng của Sao Mai Corp đang thắc mắc chưa biết up hồ sơ lưu hành sản phẩm có mục đích duy nhất là khử khuẩn ,tiệt khuẩn trang thiết bị y tế vì thế để thuận tiện cho việc up hồ sơ chúng tôi xin phép hướng dẫn cách up và các lưu ý trong quá trình kiểm tra hồ sơ. Rất mong sẽ cung cấp nhưng thông tin hữu ích về đăng ký lưu hành trang thiết bị y tế cho bạn đọc
Mục Lục Bài Viết
Hướng dẫn đăng ký lưu hành trang thiết bị y tế là sản phẩm khử khuẩn, tiệt khuẩn
Theo khoản d điều 1 nghị định 03/2020/ NĐ-CP “Bắt đầu tiếp nhận hồ sơ và cấp số đăng ký lưu hành đối với hóa chất, chế phẩm diệt côn trùng, diệt khuẩn dùng trong lĩnh vực gia dụng và y tế chỉ có một mục đích là khử khuẩn trang thiết bị y tế từ ngày 01 tháng 01 năm 2019. Số đăng ký lưu hành có hiệu lực kể từ ngày cấp” để hiểu rõ hơn thế làm thế nào để đăng ký một cách nhanh nhất chúng tôi xin diễn giải các nội dung như sau:
I. Quy định pháp lý về đăng ký lưu hành trang thiết bị y tế Căn Cứ :Nghị định số 36/2016/NĐ-CP:
1. Tại Điều 3, Nghị định số 36/2016/NĐ-CP:
Hóa chất, chế phẩm chỉ có một mục đích là khử khuẩn trang thiết bị y tế được quản lý theo quy định của Nghị định quản lý trang thiết bị y tế.
Hóa chất, chế phẩm có mục đích khử khuẩn trang thiết bị y tế nhưng ngoài ra còn có mục đích sử dụng khác được quản lý theo quy định của pháp luật về hóa chất, chế phẩm diệt côn trùng, diệt khuẩn dùng trong lĩnh vực gia dụng và y tế (Nghị định số 91/2016/NĐ-CP).
2. Thông tư số 39/2016/TT-BYT:
Sản phẩm khử khuẩn/tiệt khuẩn trang thiết bị y tế: là các trang thiết bị y tế được phân loại theo quy tắc 15, Phần II, Thông tư số 39/2016/TT-BYT ngày 28/10/2016 của Bộ Y tế quy định chi tiết việc phân loại trang thiết bị y tế.

II. Lưu ý
khi khai báo thông tin hồ sơ đăng ký lưu hành trang thiết bị y tế là: sản phẩm khử khuẩn/tiệt khuẩn. mục đích duy nhất là khử khuẩn trang thiết bị y tế trên Hệ thống dịch vụ công trực tuyến quản lý trang thiết bị y tế www.dmec.moh.gov.vn
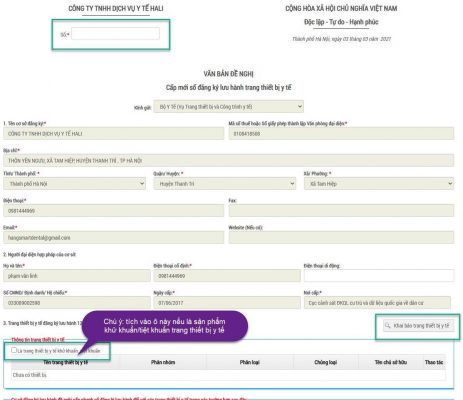
Hồ sơ kỹ thuật của Hồ sơ đăng ký lưu hành trang thiết bị y tế khử khuẩn/tiệt khuẩn trang thiết bị y tế được quy định tại Điều 26 Nghị định số 36/2016/NĐ-CP, Nghị định số 169/2018/NĐ-CP gồm:
- Tài liệu mô tả tóm tắt kỹ thuật trang thiết bị y tế bằng tiếng Việt theo Mẫu số 01 Phụ lục VIII Nghị định số 36/2016/NĐ-CP kèm theo các tài liệu chứng minh các thông tin đã nêu trong Mẫu số 01 Phụ lục VIII.
- Tài liệu hướng dẫn sử dụng của trang thiết bị y tế
- Mẫu nhãn sẽ sử dụng khi lưu hành tại Việt Nam của trang thiết bị y tế.
HƯỚNG DẪN CHI TIẾT BẢN MÔ TẢ KỸ THUẬT TRONG ĐĂNG KÝ LƯU HÀNH TRANG THIẾT BỊ Y TẾ NHƯ SAU:
| STT | Đề mục | Nội dung mô tả tóm tắt |
| 1 | Mô tả sản phẩm trang thiết bị y tế | |
| 1.1 | Mô tả trang thiết bị y tế | Mô tả tóm tắt về nguyên lý hoạt động và tính năng, thông số kỹ thuật của trang thiết bị; nêu rõ nếu trang thiết bị sử dụng các công nghệ mới thì cần cung cấp bản mô tả về công nghệ mới đó (ví dụ công
nghệ nano) |
| 1,2 | Danh mục linh kiện và phụ
kiện |
Liệt kê các linh kiện và phụ kiện của trang thiết bị y tế |
| 1,3 | Mục đích/Chỉ định sử dụng | Nêu mục đích sử dụng/chỉ định sử dụng của trang thiết bị y tế |
| 1,4 | Hướng dẫn sử dụng | Tóm tắt hướng dẫn về cách sử dụng của trang thiết bị theo như Tờ
hướng dẫn sử dụng hoặc Tờ thông tin của trang thiết bị y tế |
| 1,5 | Chống chỉ định | Thông tin về chống chỉ định – nghĩa là những trường hợp không được chỉ định sử dụng trang thiết bị vì lý do an toàn cho người bệnh, ví dụ do tiền sử bệnh, đặc điểm sinh lý của người bệnh, vv…; theo đúng nội dung đã được duyệt tại nước sản xuất và có ghi trên nhãn trang
thiết bị y tế |
| 1,6 | Cảnh báo và thận trọng | Những thông tin cảnh báo và những điểm cần thận trọng khi sử dụng trang thiết bị y tế, kể cả những biện pháp dự phòng để bảo vệ người bệnh tránh những rủi ro do sử dụng trang thiết bị y tế; đó có thể là thông tin cảnh báo về tác dụng bất lợi hay sử dụng sai và biện pháp
ngăn ngừa |
| 1,7 | Tác dụng bất lợi có thể xảy ra | Thông tin về các tác dụng bất lợi liên quan đến sử dụng trang thiết bị y tế được ghi nhận qua thử nghiệm lâm sàng và theo dõi hậu mại đã
được thực hiện trước đó đối với trang thiết bị y tế |
| 2 | Thông tin sản phẩm đã lưu hành tại các nước (nếu có)
Cung cấp thông tin về các nước đã phê duyệt cho phép lưu hành sản phẩm, nước đầu tiên cấp đăng ký/cho phép lưu hành trang thiết bị y tế |
| 3 | Chỉ định đã đăng ký ở các nước khác (nếu có)
Liệt kê các nước đã cấp đăng ký lưu hành đi kèm với chỉ định sử dụng được phê duyệt tại nước đó; ngày được cấp đăng ký |
| 4 | Thông tin về tính an toàn/ vận hành đáng lưu ý của sản phẩm trang thiết bị y tế
– Cung cấp thông tin về số lượng báo cáo phản ứng bất lợi liên quan đến việc sử dụng trang thiết bị y tế; Những biện pháp thu hồi/ điều chỉnh hậu mại đã thực hiện theo yêu cầu của cơ quan quản lý các nước; – Nếu trang thiết bị y tế có chứa một trong các thành phần sau, thì cần cung cấp thông tin về:
|
*Lưu ý:
Mục 1.1
a. Thành phần của sản phẩm:
– Thông tin các chất có hoạt tính khử khuẩn kèm hàm lượng, nhà sản xuất.
– Thông tin các thành phần phụ khác của sản phẩm kèm hàm lượng.
b. Đặc tính lý hóa của chế phẩm (nếu có): Tỷ trọng với chất lỏng; Khả năng bắt
lửa, điểm chớp; Khả năng ăn mòn; Độ bền bảo quản; Độ acid, kiềm hoặc pH;
Khả năng hỗn hợp với chế phẩm khác.
c. Hiệu lực sinh học của chế phẩm:
– Cơ chế tác động của chế phẩm để tiệt khuẩn/khử khuẩn.
– Khả năng tiệt khuẩn/khử khuẩn (chủng loại vi khuẩn).
– Liều lượng sử dụng.
– Khoảng thời gian giữa các lần sử dụng (đối với chế phẩm có tác dụng tồn lưu)
– Môi trường pha loãng nếu có (nước, dầu…)
– Phương pháp sử dụng.
d. Dạng chế phẩm.
e. Điều kiện bảo quản
g. Hạn sử dụng.
Các tài liệu chứng minh các thông tin đã nêu trong Mục 1.1
- Tài liệu liên quan đến thành phần, hàm lượng các chất có hoạt tính khử khuẩn như: Phiếu kiểm nghiệm hoạt chất; Bản mô tả hàm lượng, thành phần hoạt chất.
- Tài liệu liên quan đến hiệu lực sinh học của sản phẩm như: Tài liệu nghiên cứu, đánh giá hiệu lực sinh học của sản phẩm; Kết quả khảo nghiệm đánh giá hiệu lực sinh học của sản phẩm.
Mục 1.6. Cảnh báo và thận trọng, gồm các thông tin:
a. Các thông tin đánh giá tương thích sinh học của sản phẩm như:
- Các thông tin đánh giá độc tính của sản phẩm như: Độc cấp tính qua miệng (LD50); độc cấp tính qua da (LD50); độc cấp tính qua hô hấp (LC50); khả năng kích thích mắt; khả năng kích thích da; khả năng gây dị ứng.
- Các thông tin về độc tính sinh thái, khả năng phân hủy và tồn dư.
b. Các thông tin liên quan đến độc cấp tính; độc bán trường diễn/ trường diễn; độc mãn tính; khả năng gây đột biến gen; khả năng gây ung thư; độc tính với sinh sản và sự phát triển; khả năng chuyển hóa trong môi trường; độc tính sinh thái của chất có hoạt tính khử khuẩn (đối với trang thiết bị y tế loại C không phải dung dịch làm sạch, ngâm, rửa hoặc dưỡng ẩm kính áp tròng)
c. Các thông tin y khoa, triệu chứng ngộ độc, thuốc giải độc (nếu có).
d. Các thông tin khác như phương pháp tiêu hủy chế phẩm hết hạn hoặc không sử dụng hết; phương pháp tiêu hủy bao gói chế phẩm.
Các tài liệu chứng minh các thông tin đã nêu trong mục 1.6. mẫu số 01 Phụ lục VIII gồm:
- Tài liệu đánh giá tương thích sinh học của sản phẩm.
- Phiếu an toàn hóa chất đối với những sản phẩm phải lập Phiếu an toàn hóa chất theo quy định của pháp luật về hóa chất.
Đối với các sản phẩm đã được Bộ Y tế Việt Nam (Cục Quản lý môi trường y tế) cấp số đăng ký lưu hành:
- Các tài liệu chứng minh các thông tin đã nêu trong mẫu số 01 Phụ lục VIII gồm:
- Giấy phép lưu hành đã được Bộ Y tế Việt Nam cấp.
- Các tài liệu liên quan đến kiểm nghiệm thành phần, hàm lượng các chất có hoạt tính khử khuẩn; kết quả khảo nghiệm đánh giá hiệu lực sinh học của sản phẩm; phiếu an toàn hóa chất của sản phẩm đã nộp trong hồ sơ đã được cấp phép trước đây.
Ngoài các yêu cầu chung như các trang thiết bị y tế chung khác thì cần phải nêu rõ:
- Mục đích sử dụng, tác dụng cụ thể của sản phẩm (tiệt khuẩn; khử khuẩn mức độ cao; khử khuẩn mức độ trung bình; khử khuẩn mức độ thấp; làm sạch; khử
nhiễm…)
- Miêu tả được các bước trong quá trình sử dụng.
- Hướng dẫn an toàn và xử lý khi sử dụng sản phẩm.
- Cảnh báo thận trọng.
- Tác dụng không mong muốn.
- Quy cách đóng gói Trang thiết bị y tế nhập khẩu vào Việt Nam: nhãn gốc chưa thể hiện hoặc thể hiện chưa đủ những nội dung theo quy định thì phải có nhãn phụ thể hiện những nội dung bắt buộc bằng tiếng Việt và giữ nguyên nhãn gốc của hàng hoá.
Nhãn sản phẩm khử khuẩn/tiệt khuẩn trang thiết bị y tế: Ngoài các yêu cầu chung như các trang thiết bị y tế khác thì cần phải ghi rõ thông tin cảnh báo thận trọng.
Ngoài ra còn rất nhiều vấn đề liên quan đến việc đăng ký lưu hành trang thiết bị y tế hãy liên hệ với Sao Mai Corp để được tư vấn miễn phí Hotline :+84 92 4444 992 ( Mr Trung)
Mọi thông tin chi tiết xin vui lòng liên hệ:
CÔNG TY CỔ PHẦN PHÁT TRIỂN QUỐC TẾ SAO MAI
Hotline : +84 92 4444 992
Email : info@saomaicorp.com.vn
Office : Tầng 10 Tòa nhà Sico, Số 2, Ngõ 2, Đường Nguyễn Hoàng, Quận Nam Tư Liêm, Thành Phố Hà Nội,VN
Website : Saomaicorp.com.vn