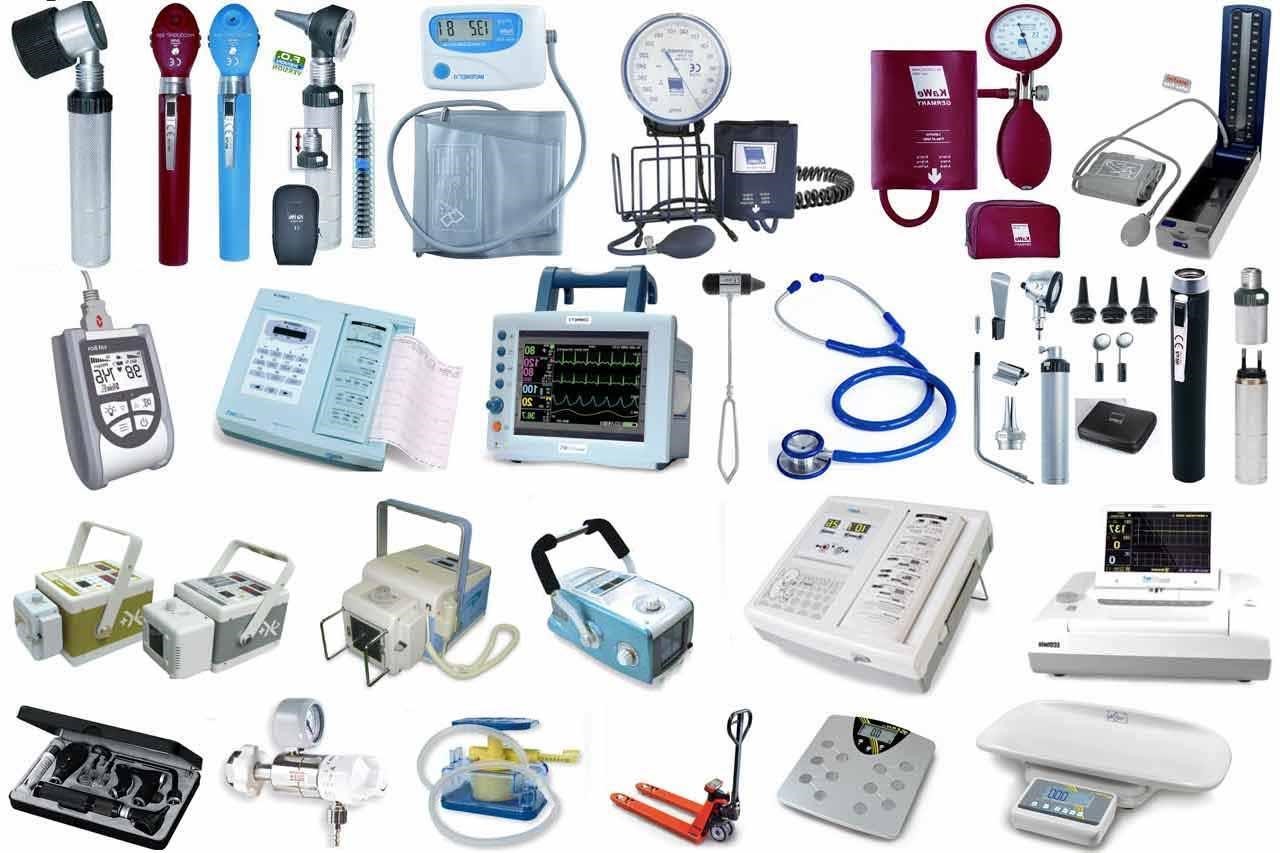
Cùng Sao Mai Corp tìm hiểu về điều kiện đăng ký lưu hành trang thiết bị y tế. Các loại giấy tờ làm hồ sơ đăng ký lưu hành trang thiết bị y tế ngay trong bài viết dưới đây. Thông qua thông chia sẻ này mong rằng sẽ hữu ích với mọi người, giúp mọi người có được sự chuẩn bị tốt nhất cho hoạt động kinh doanh nhập khẩu của mình nhé!
Mục Lục Bài Viết
Điều kiện đăng ký lưu hành trang thiết bị y tế
Điều kiện để cấp giấy chứng nhận đăng ký lưu hành trang thiết bị y tế:
- Được sản xuất tại cơ sở đã công bố đủ điều kiện sản xuất đối với trang thiết bị y tế sản xuất trong nước;
- Được sản xuất tại cơ sở đã được cấp Giấy chứng nhận đạt tiêu chuẩn quản lý chất lượng và được lưu hành tại bất kỳ quốc gia nào trên thế giới đối với trang thiết bị y tế nhập khẩu;
- Phù hợp với quy chuẩn kỹ thuật quốc gia hoặc tiêu chuẩn mà nhà sản xuất công bố áp dụng.
Không cho phép thực hiện đăng ký lưu hành đối với trang thiết bị y tế thuộc một trong các trường hợp sau:
- Trang thiết bị y tế thuộc trường hợp theo quy định tại khoản 1 Điều 34 Nghị định này;
- Trang thiết bị y tế bị thu hồi thuộc trường hợp theo quy định tại các khoản 1 và 3 Điều 35 Nghị định này.
Không tiếp nhận hồ sơ công bố tiêu chuẩn áp dụng hoặc đăng ký lưu hành trong thời hạn 12 tháng, kể từ ngày có quyết định thu hồi số đăng ký lưu hành đối với trang thiết bị y tế thuộc một trong các trường hợp theo quy định tại các khoản 2 và 8 Điều 35 Nghị định này.
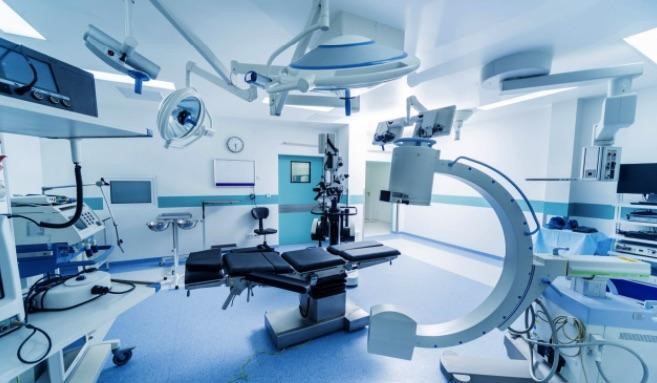
Hồ sơ thủ tục đăng ký lưu hành trang thiết bị y tế hợp pháp
Hồ sơ đăng ký lưu hành trang thiết bị y tế chưa có quy chuẩn kỹ thuật quốc gia
- Văn bản đề nghị cấp mới số lưu hành theo Mẫu ;
- Bản phân loại trang thiết bị y tế theo mẫu ;
- Giấy chứng nhận đạt tiêu chuẩn quản lý chất lượng còn hiệu lực tại thời điểm nộp hồ sơ;
- Giấy ủy quyền của chủ sở hữu trang thiết bị y tế cho cơ sở thực hiện việc đăng ký lưu hành theo mẫu;
- Giấy xác nhận đủ điều kiện bảo hành do chủ sở hữu trang thiết bị y tế cấp theo mẫu, trừ trường hợp trang thiết bị y tế sử dụng một lần theo quy định của chủ sở hữu trang thiết bị y tế hoặc có tài liệu chứng minh không có chế độ bảo hành;
- Giấy chứng nhận lưu hành tự do còn hiệu lực tại thời điểm nộp hồ sơ đối với trang thiết bị y tế nhập khẩu;
- Tài liệu mô tả tóm tắt kỹ thuật trang thiết bị y tế bằng tiếng Việt theo mẫu kèm theo tài liệu kỹ thuật mô tả chức năng, thông số kỹ thuật của trang thiết bị y tế do chủ sở hữu trang thiết bị y tế ban hành;
Tài liệu mô tả tóm tắt kỹ thuật trang thiết bị y tế bằng tiếng Việt theo mẫu kèm theo tài liệu kỹ thuật mô tả chức năng, thông số kỹ thuật của trang thiết bị y tế do chủ sở hữu trang thiết bị y tế ban hành;
Chú ý: Riêng đối với thuốc thử, chất hiệu chuẩn, vật liệu kiểm soát in vitro: tài liệu kỹ thuật bằng tiếng Việt theo Mẫu số 02 quy định tại Phụ lục VIII ban hành kèm theo Nghị định này kèm theo tài liệu về nguyên vật liệu, về an toàn của sản phẩm, quy trình sản xuất, các báo cáo nghiên cứu lâm sàng và tiền lâm sàng bao gồm báo cáo độ ổn định;
- h) Hồ sơ kỹ thuật chung thực hiện theo hướng dẫn tại Hiệp định ASEAN về trang thiết bị y tế;
- i) Tài liệu hướng dẫn sử dụng của trang thiết bị y tế;
- k) Đối với trang thiết bị y tế thuộc loại C, D có xâm nhập cơ thể người: Bản tóm tắt dữ liệu thử lâm sàng theo mẫu kèm theo kết quả nghiên cứu thử lâm sàng, trừ các trường hợp sau:
- Trang thiết bị y tế đã được lưu hành và cấp giấy chứng nhận lưu hành tự do của một trong các nước sau: các nước thành viên EU, Nhật Bản, Canada, Úc (TGA), Mỹ (FDA);
- Trang thiết bị y tế đã được cấp lưu hành trước khi Nghị định này có hiệu lực;
- Các trường hợp khác theo quy định của Bộ trưởng Bộ Y tế.
- l) Đối với trang thiết bị y tế chẩn đoán in vitro thuộc loại C, D phải có thêm giấy chứng nhận kiểm định theo quy định của Bộ trưởng Bộ Y tế, trừ các trường hợp sau:
- Trang thiết bị y tế đã được cấp giấy chứng nhận lưu hành tự do của một trong các nước sau: các nước thành viên EU, Nhật Bản, Canada, Úc (TGA), Mỹ (FDA);
- Trang thiết bị y tế đã được cấp lưu hành trước khi Nghị định này có hiệu lực;
- m) Mẫu nhãn sẽ sử dụng khi lưu hành tại Việt Nam của trang thiết bị y tế;
- n) Phiếu tiếp nhận hồ sơ công bố đủ điều kiện sản xuất phù hợp với sản phẩm xin cấp số đăng ký lưu hành đối với trang thiết bị y tế sản xuất trong nước;
- o) Báo cáo kết quả hoạt động kinh doanh trong thời hạn được cấp số lưu hành theo Mẫu đối với trang thiết bị y tế đã được cấp lưu hành trước khi Nghị định này có hiệu lực thi hành thuộc diện miễn nộp bản tóm tắt dữ liệu thử lâm sàng hoặc miễn giấy chứng nhận kiểm định.
Hồ sơ đăng ký lưu hành trang thiết bị y tế có quy chuẩn kỹ thuật quốc gia
- a) Văn bản đề nghị cấp mới số đăng ký lưu hành theo mẫu ;
- b) Giấy chứng nhận hợp quy;
- c) 20 Giấy tờ theo quy định tại các điểm b, c, d, đ, e, g, h, i, m, n và o khoản 1 Điều này.
Hồ sơ đề nghị cấp mới số lưu hành đối với trang thiết bị y tế là phương tiện đo phải phê duyệt mẫu theo quy định của pháp luật về đo lường
- a) Văn bản đề nghị cấp mới số đăng ký lưu hành theo mẫu;
- b) Quyết định phê duyệt mẫu;
- c) Giấy tờ theo quy định tại các điểm b, c, d, đ, e, g, h, i, m, n và o khoản 1 Điều này.
Trên đây các loại giấy tờ, hồ sơ đăng ký lưu hành trang thiết bị y tế mà Sao Mai Corp muốn chia sẻ đến mọi người, để nhận tư vấn và hỗ trợ đăng ký lưu hành trang thiết bị y tế từ A-Z hãy liên hệ đến Sao Mai Corp qua thông tin bên dưới nhé!
Mọi thông tin chi tiết vui lòng liên hệ
CÔNG TY CỔ PHẦN PHÁT TRIỂN QUỐC TẾ SAO MAI
Hotline: +84 924 444 992
Email: info@saomaicorp.com.vn
Địa chỉ: Tầng 10 Tòa nhà Sico, Số 2, Ngõ 2, Đường Nguyễn Hoàng, Quận Nam Từ Liêm, Thành Phố Hà Nội, Việt Nam.