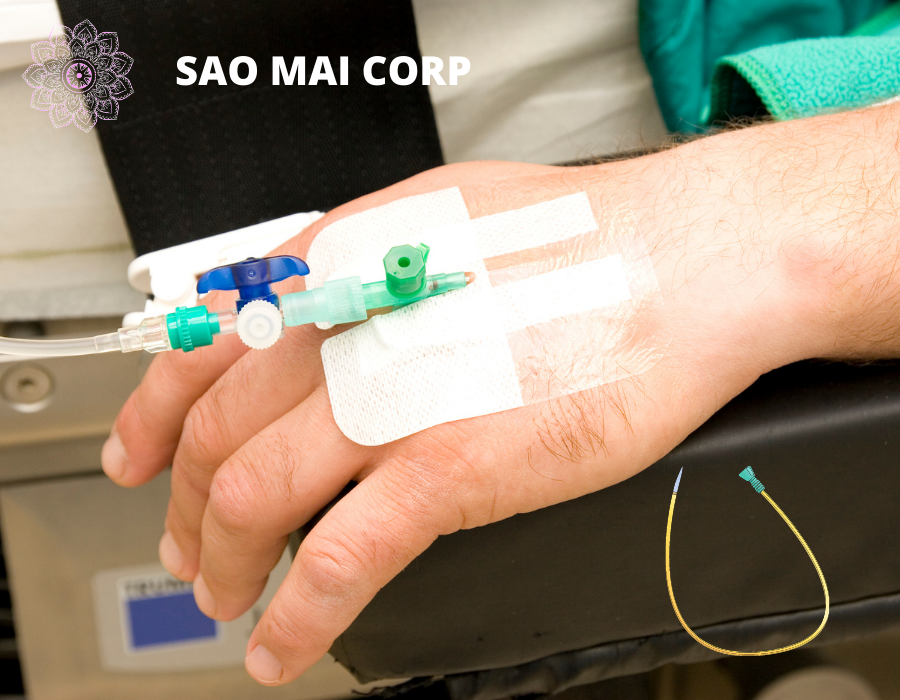
Đăng ký lưu hành Ống thông tĩnh mạch
Bạn đang muốn đăng ký lưu hành Ống thông tĩnh mạch?
Đăng ký lưu hành Ống thông tĩnh mạch cần chuẩn bị những hồ sơ gì?
Lưu ý khi đăng ký lưu hành Ống thông tĩnh mạch!
Thủ tục nhập khẩu Ống thông tĩnh mạch như thế nào?
Thời gian đăng ký lưu hành Ống thông tĩnh mạch mất bao lâu?
Qua bài viết này Sao Mai Corp sẽ giải đáp cho bạn đọc những thắc mắc trên. Sao Mai Corp chuyên vận chuyển hàng và thông quan hàng hóa trang thiết bị y tế. Hotline tư vấn miễn phí 24/7: 092 4444 992
- Căn cứ nghị định số Nghị định số 36/2016/NĐ-CP.
- Căn cứ nghị định 169/2018/NĐ-CP
Ống thông tĩnh mạch là trang thiết bị Y tế nhập khẩu chưa có quy chuẩn quốc gia tương ứng, Bước đầu tiên để nhập khẩu cũng như đăng ký lưu hành trang thiết bị y tế cần phải phân loại trang thiết bị y tếB
Ống thông tĩnh mạch là thiết bị y tế phân loại: B
I. Thủ tục đăng ký lưu hành Ống thông tĩnh mạch.
Chuẩn bị hồ sơ:
- Bảng phân loại trang thiết bị y tế.
- Giấy chứng nhận tiêu chuẩn quản lý chất lượng (ISO 13485)
- Giấy chứng nhận lưu hành tự do còn hiệu lực tại thời điểm nộp hồ sơ đối với trang thiết bị y tế nhập khẩu hoặc Phiếu tiếp nhận hồ sơ công bố đủ điều kiện sản xuất trang thiết bị y tế đối với TTBYT sản xuất trong nước(CFS).
- Giấy xác nhận đủ điều kiện bảo hành.
- Thư ủy quyền của chủ sở hữu trang thiết bị y tế (LOA)
- Mẫu nhãn mác tại lưu hành tại Việt Nam
- Catalog sản phẩm
Quy trình up hồ sơ xin đăng ký lưu hành Ống thông tĩnh mạch
- Up hồ sơ lên website quản lý của bộ y tế là: https://dmec.moh.gov.vn/
- Đóng phí nhà nước
- Chờ vụ trang thiết bị y tế xem hồ sơ và phê duyệt lưu hành
- Thời gian phê duyệt là 30-90 ngày làm việc có thể lâu hơn tùy thuộc vào tính chính xác hồ sơ.
Lưu ý:
– Giấy chứng nhận đạt tiêu chuẩn quản lý chất lượng còn hiệu lực tại thời điểm nộp hồ sơ, trừ trường hợp trang thiết bị y tế đã được cấp giấy chứng nhận lưu hành tự do của một trong các nước hoặc tổ chức sau: Các nước thành viên EU, Nhật Bản, Ca-na-đa, TGA của Úc, FDA của Mỹ (Nộp bản gốc hoặc bản sao có chứng thực hoặc bản sao có xác nhận của cơ sở đề nghị cấp số lưu hành. Trường hợp nộp bản sao có xác nhận của cơ sở đề nghị cấp số lưu hành thì khi nộp hồ sơ phải xuất trình bản gốc để đối chiếu hoặc cung cấp nguồn dữ liệu để cơ quan tiếp nhận hồ sơ tra cứu về tính hợp lệ của các giấy tờ này. Trường hợp Giấy chứng nhận đạt tiêu chuẩn quản lý chất lượng không bằng tiếng Anh hoặc không bằng tiếng Việt thì phải dịch ra tiếng Việt. Bản dịch phải được chứng thực theo quy định của pháp luật);
– Giấy ủy quyền của chủ sở hữu trang thiết bị y tế cho cơ sở thực hiện việc đăng ký lưu hành theo mẫu quy định tại Phụ lục VI ban hành kèm theo Nghị định 36/2016/NĐ-CP còn hiệu lực tại thời điểm nộp hồ sơ, trừ trường hợp theo quy định tại điểm a khoản 1 Điều 21 Nghị định 36/2016/NĐ-CP (Đối với trang thiết bị y tế nhập khẩu: Nộp bản đã được hợp pháp hóa lãnh sự hoặc bản sao có chứng thực của bản đã được hợp pháp hóa lãnh sự);
– Giấy xác nhận đủ điều kiện bảo hành do chủ sở hữu trang thiết bị y tế cấp theo mẫu quy định tại Phụ lục VII ban hành kèm theo Nghị định 36/2016/NĐ-CP, trừ trường hợp trang thiết bị y tế sử dụng một lần theo quy định của chủ sở hữu trang thiết bị y tế;
– Giấy chứng nhận lưu hành tự do còn hiệu lực tại thời điểm nộp hồ sơ đối với trang thiết bị y tế nhập khẩu (Nộp bản đã được hợp pháp hóa lãnh sự hoặc bản sao có chứng thực của bản đã được hợp pháp hóa lãnh sự. Trường hợp giấy chứng nhận lưu hành tự do không bằng tiếng Anh hoặc không bằng tiếng Việt thì phải dịch ra tiếng Việt. Bản dịch phải được chứng thực theo quy định của pháp luật. Trường hợp giấy chứng nhận lưu hành tự do không ghi rõ thời hạn hết hiệu lực thì thời điểm hết hết hiệu lực của giấy chứng nhận lưu hành tự do được tính là 36 tháng, kể từ ngày cấp).;
– Tài liệu mô tả tóm tắt kỹ thuật trang thiết bị y tế bằng tiếng Việt theo mẫu số 01 quy định tại Phụ lục VIII ban hành kèm theo Nghị định 36/2016/NĐ-CP
– Tài liệu kỹ thuật (catalogue) mô tả chức năng, thông số kỹ thuật của trang thiết bị y tế; Tài liệu kỹ thuật đối với thuốc thử, chất hiệu chuẩn, vật liệu kiểm soát in vitro theo mẫu số 02 quy định tại Phụ lục VIII ban hành kèm theo Nghị định 36/2016/NĐ-CP (Nộp bản có xác nhận của cơ sở đề nghị cấp số lưu hành. Trường hợp tài liệu kỹ thuật không bằng tiếng Anh hoặc không bằng tiếng Việt, thì phải dịch ra tiếng Việt. Bản dịch phải được chứng thực theo quy định của pháp luật);
– Tài liệu hướng dẫn sử dụng của trang thiết bị y tế (Nộp bản bằng tiếng Việt có xác nhận của cơ sở đề nghị cấp số lưu hành);
– Mẫu nhãn sẽ sử dụng khi lưu hành tại Việt Nam của trang thiết bị y tế (Nộp bản mẫu nhãn có xác nhận của tổ chức đứng tên đăng ký lưu hành. Mẫu nhãn phải đáp ứng các yêu cầu theo quy định tại Điều 54 Nghị định 36/2016/NĐ-CP).
II. Thủ tục nhập khẩu Ống thông tĩnh mạch
Chuẩn bị hồ sơ:
- Hóa đơn thương mại (Invoice)
- BILL tàu
- Giấy lưu hành Ống thông tĩnh mạch.
- Phân loại trang thiết bị y tế.
Các bước tiến hành và lưu ý:
Tên hàng và mã HS code:
| Mã hs code tham khảo | Tên hàng tham khảo | Thuế nhập khẩu | Thuế VAT |
| 90181900 | Ống thông tĩnh mạch AHF8 Model xxx, Diopter +1D, hãng sản xuất; XXX, xuất xứ: XXX, |
0% | 5% |
- Khai báo hải quan điện tử
- Đóng thuế và thông quan hàng hóa.
Lưu ý:
- Không chỉ với thủ tục nhập Ống thông tĩnh mạch các trang thiết bị y tế khác cũng phải kiểm tra thật kỹ hồ sơ, khai báo tên hàng như trong phân loại và lưu hành đã được cấp. Trên bao bì của hàng hóa phải ghi rõ và đầy đủ nội dung: Tên hàng, model, chủng loại, nhà sản xuất, chủ sở hữu, Nước sản xuất.
- Tất cả các giấy tờ đăng ký lưu hành Ống thông tĩnh mạch phải luôn có hiệu lực.
- Nếu thành phần trên nhãn gốc của sản phẩm không khớp giấy tờ lưu hành thủy tinh thể và phân loại. Doanh nghiệp sẽ bị xử phạt hành chính từ 30 đến 50 triệu đồng và trong vòng 30 ngày kể từ ngày xử phạt. Doanh nghiệp phải bổ sung được lưu hành mới. Nếu quá 30 ngày, Doanh nghiệp không xuất trình được công lưu hành, hải quan sẽ tiến hành thủ tục tái xuất lô hàng.
Trên đây là bài viết của chúng tôi về thủ tục đăng ký lưu hành Ống thông tĩnh mạch và thủ tục nhập khẩu Ống thông tĩnh mạch.
Quý khách hàng có thắc mắc hoặc có nhu cầu sử dụng dịch vụ của Sao Mai corp . Hãy liên hệ với chúng tôi ngay để được tư vấn miễn phí qua Hotline: +84 92 4444 992
CÔNG TY CỔ PHẦN PHÁT TRIỂN QUỐC TẾ SAO MAI
Hotline : +84 924 444 992
Email: info@saomaicorp.com.vn
Địa chỉ: Tầng 10 Tòa nhà Sico, Số 2, Ngõ 2, Đường Nguyễn Hoàng, Quận Nam Từ Liêm, Thành Phố Hà Nội, Việt Nam.
Tư vấn nhập khẩu thiết bị y tế từ A-Z